Cycle cellulaire
Reproduction cellulaire : mitose
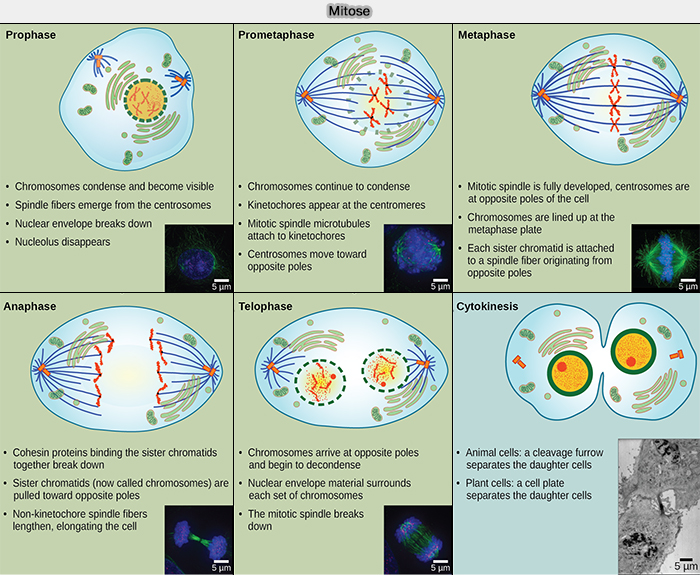
Prophase
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

La prophase inaugure la mitose par la condensation des chromosomes, la maturation des centrosomes et la mise en place progressive du fuseau mitotique.
La prophase est la première phase morphologiquement identifiable de la mitose, au cours de laquelle la cellule réorganise son architecture nucléaire et cytoplasmique pour préparer la ségrégation des chromatides soeurs.
(Figure : vetopsy.fr d'après Opened-cuny.edu)
Événements cellulaires de la prophase
1. La condensation chromosomique transforme la chromatine répliquée en structures compactes et individualisées, rendant visibles les chromatides sœurs, grâce à l’activation des complexes condensines I et II et à la phosphorylation des histones H1 et H3.
Cette compaction :
- réduit la fragilité mécanique de l’ADN pendant la ségrégation,
- prépare la formation de bras chromosomiques manipulables.

La condensation chromosomique, les condensines et les cohésines sont étudiées dans des chapitres spécifiques.
2. Les centrosomes, maturés en fin de G2 et séparés en début de prophase, organisent les premiers microtubules du fuseau mitotique, grâce à l’expansion du matériel péricentriolaire (PCM) par enrichissement via des protéines d’échafaudage telles que PCNT (péricentrine), CEP192 et CDK5RAP2 (CEP215) et au recrutement accru des complexes γ-TuRC.
- Cette séparation est indispensable pour orienter correctement les forces mécaniques de la métaphase.
- Elle se poursuit fonctionnellement en anaphase B par l’écartement actif des pôles.
3. Les microtubules commencent à se former en réseaux radiaires autour des centrosomes, établissant une structure préliminaire qui préfigure le fuseau mitotique, sous l’influence coordonnée des γ-TuRC et de MAP péricentriolaires comme XMAP215/ch-TOG, NEDD1 (GCP-WD) et CDK5RAP2.
Les microtubules polaires s’allongent vers la région nucléaire, anticipant la capture des chromosomes après la rupture de l’enveloppe nucléaire.
4. Le noyau entame une phase de déstabilisation, avec le début de la désorganisation des lamines A/C et B qui soutiennent l’enveloppe nucléaire, par phosphorylation dépendante de l’activité cycline B/CDK1 (MPF).
Cette transition rend possible la rupture complète de l’enveloppe en prométaphase.
5. Les centromères s’organisent pour permettre l’assemblage ultérieur des kinétochores, structures qui ne seront pleinement fonctionnelles qu’après la rupture nucléaire, par stabilisation du nucléosome CENP-A/H4 et organisation du réseau CCAN (Constitutive Centromere-Associated Network).
La mise en place du CCAN et des précurseurs du complexe KMN (KNL1-Mis12-Ndc80) prépare l’assemblage ultérieur de kinétochores fonctionnels après la rupture de l’enveloppe nucléaire.
Régulations moléculaires de la prophase
Les transformations morphologiques observées au cours de la prophase sont déclenchées par l’entrée de la cellule dans un état mitotique global, imposé par l’activation coordonnée de régulateurs enzymatiques déjà engagés en fin de G2.
Activation du MPF et préparation nucléaire
1. L’activation du complexe cycline B/CDK1 (MPF) constitue le moteur de cette transition et explique l’apparition coordonnée des principaux caractères de la prophase (
Elle entraîne :
- l'amorce de la condensation chromosomique par la phosphorylation des histones H1 et H3 et des condensines,
- la maturation progressive des centrosomes pour la formation du fuseau mitotique, par phosphorylation de protéines du matériel péricentriolaire (PCM), notamment CEP192, NEDD1 (GCP-WD), PCNT (péricentrine) et CDK5RAP2 (CEP215)
- la déstabilisation progressive de l’enveloppe nucléaire par la phosphorylation des lamines A/C et B.
2. En fin de prophase, l’augmentation locale de l’activité mitotique dans le noyau prépare la rupture de l’enveloppe nucléaire, événement qui marque le passage à la prométaphase.
3. Les kinases Plk1 et Aurora A amplifient la propagation du signal MPF, accélérant la transition vers la prométaphase (
Contrôles de progression et surveillance
1. Le complexe APC/C (Anaphase-Promoting Complex/Cyclosome) demeure fonctionnellement inactif, l’absence d’activation par Cdc20 ou Cdc20 étant maintenue par la phosphorylation inhibitrice de ses sous-unités par les kinases mitotiques actives.
Cette inactivation précoce :
- empêche toute dégradation prématurée des substrats mitotiques, notamment la sécurine et la cycline B,
- prépare la bascule métaphase/anaphase qui ne surviendra qu’après la levée du SAC.
2. Le point de contrôle du fuseau (SAC ou Spindle Assembly Checkpoint) reste silencieux durant la prophase, car les kinétochores ne sont pas encore accessibles aux microtubules tant que l’enveloppe nucléaire demeure intacte (
Cette absence d’activation :
- empêche la formation du complexe MCC (Mitotic Checkpoint Complex), qui n’apparaîtra qu’en prométaphase,
- laisse Cdc20 momentanément libre mais incapable d’activer l’APC/C.
Passage à la prométaphase
La prométaphase débute lorsque l’enveloppe nucléaire se rompt, exposant les kinétochores au fuseau et initiant la capture des chromosomes.
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


