Cycle cellulaire
Enzymes mitotiques majeures
Vue d'ensemble
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

Les enzymes mitotiques coordonnent l’assemblage, la surveillance et le démantèlement du fuseau mitotique en orchestrant l’équilibre dynamique entre phosphorylations et déphosphorylations au cours de la mitose.
Cette page a pour rôle de présenter la logique enzymatique globale de la mitose, sans redévelopper les mécanismes moléculaires détaillés, qui sont traités dans des pages dédiées.
Elle articule :
- les kinases mitotiques majeures, qui initient, amplifient et coordonnent les événements de la mitose en aval du complexe cycline B/CDK1 (MPF),
- les phosphatases impliquées dans la sortie de mitose, responsables de l’extinction progressive des phosphorylations mitotiques,
- Les ligases E3 (APC/C, SCF), qui imposent l’irréversibilité temporelle des transitions mitotiques en déclenchant la dégradation ciblée des cyclines, des sécurines et d’autres régulateurs clés,
- la coordination temporelle de ces activités enzymatiques avec les complexes cyclines/CDK et l’architecture du fuseau mitotique.
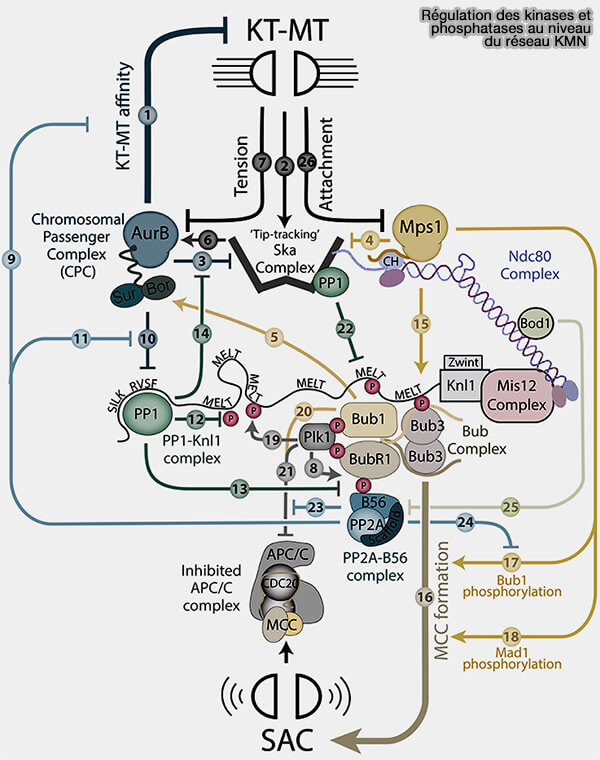
(Figure : vetopsy.fr d'après Saurin)
Remarque : cette figure est issue de l’article Kinase and Phosphatase Cross-Talk at the Kinetochore (2018).
- L’activation initiale de Plk1 par Aurora A (via Bora) n’est pas représentée dans ce schéma, qui se concentre sur les interactions kinases/phosphatases au kinétochore.
- Sans l'article, les voies de régulation numérotées sont détaillées.
Principes généraux de la régulation enzymatique de la mitose
1. La mitose est contrôlée par un réseau coordonné de kinases et de phosphatases dont l’activité varie selon les phases.
- Le complexe cycline B/CDK1 (MPF) constitue le moteur central de l’entrée, du maintien et de la sortie de mitose, tandis que les autres complexes cycline/CDK participent à la préparation et à la coordination temporelle du cycle cellulaire.
Les CDK interphasiques conditionnent l’état préalable de la cellule, le complexe cycline A/CDK1 participe à la préparation et à la prométaphase.
- Les kinases mitotiques spécialisées (Plk1, Aurora A, Aurora B) assurent l’organisation spatiale du fuseau, le contrôle des attachements et la synchronisation des transitions (The role of mitotic kinases in coupling the centrosome cycle with the assembly of the mitotic spindle (2014).
- Les phosphatases PP1 et PP2A orchestrent la sortie de mitose par inversion progressive des phosphorylations mitotiques.
2. Le tableau ci-dessous fournit une vue d’ensemble fonctionnelle des enzymes mitotiques.
Les mécanismes moléculaires détaillés, structures, substrats précis et régulations fines sont développés dans les pages dédiées à chaque enzyme.
| Enzyme/ complexe |
Localisation dominante |
Phase(s) clé(s) |
Fonction mitotique principale |
|---|---|---|---|
| Kinases | |||
| Cycline B/ CDK1 |
|
Prophase ➞ anaphase |
|
| Plk1 |
|
Prophase ➞ télophase |
|
| Aurora A |
|
Prophase ➞ métaphase |
|
| Aurora B (CPC) |
Centromère ➞ kinétochore ➞ zone médiane |
Prométaphase ➞ métaphase |
|
| Ligase E3 | |||
| APC/CCdc20 |
|
Métaphase- anaphase |
Déclenchement de l'anaphase (dégradation sécurine, cycline B) |
| APC/CCdh1 |
|
Télophase ➞ G1 |
|
| SCF (Skp1–Culline –F-box) |
|
|
|
| Phosphatases | |||
| PP2A-B56 |
|
Métaphase ➞ anaphase |
|
| PP2A-B55 |
|
Anaphase ➞ télophase |
|
| PP1 |
|
Télophase |
|
Coordination enzymatique avec le fuseau mitotique
1. La dynamique et la stabilité du fuseau mitotique reposent sur la coordination étroite entre plusieurs kinases aux fonctions complémentaires.
a. Plk1 et Aurora A structurent et stabilisent l’architecture bipolaire du fuseau en contrôlant :
- la maturation des pôles centrosomaux,
- la nucléation et la dynamique des microtubules.
b. Aurora B, au sein du CPC (Chromosomal Passenger Complex), ajuste en parallèle la qualité des attachements kinétochoriens en fonction de la tension mécanique, assurant la correction des erreurs et le maintien du point de contrôle du fuseau (SAC).

Le fuseau mitotique et les interactions avec les enzymes mitotiques lors des différentes phases sont étudiés dans un chapitre spécifique.
2. Bien que spatialement distinctes, ces activités enzymatiques sont fonctionnellement couplées et maintenues sous la dépendance de l’activité du complexe cycline B/CDK1 (MPF), garantissant un état mitotique stable jusqu’au déclenchement coordonné de la sortie de mitose.
Sortie de mitose : bascule kinases-phosphatases
et réinitialisation cellulaire
La sortie de mitose correspond à une transition enzymatique irréversible, imposée par l’activation coordonnée de la protéolyse dépendante de l’APC/C et par l’inversion du rapport kinases/phosphatases.
1. La transition métaphase-anaphase est initiée par l’activation de l’APC/CCdc20 qui entraîne la dégradation simultanée de la sécurine et de la cycline B.
La destruction de la cycline B provoque l’extinction rapide de l’activité du complexe cycline B/CDK1 (MPF), constituant le signal central de la sortie de mitose.

Cette extinction de CDK1 lève les mécanismes inhibiteurs pesant sur les phosphatases PP1 et PP2A et rend possibles des événements de déphosphorylation à grande échelle.
2. La levée du point de contrôle du fuseau et l’initiation de la sortie de mitose reposent sur l’action séquentielle des phosphatases PP2A et PP1.
a. En métaphase tardive, PP2A-B56, associée à BubR1 au niveau des kinétochores, déphosphoryle les composants du réseau Bub.
Cette action favorise la dissociation progressive des complexes inhibiteurs du SAC et permet la libération de Cdc20, conditionnant l’activation complète de l’APC/CCdc20 (
b. Après l’entrée en anaphase et l’extinction rapide de l’activité du complexe cycline B/CDK1 (MPF), PP2A-B55 devient prédominante et initie l’inversion à grande échelle des phosphorylations dépendantes des CDK.
PP1 et PP2A-B55 déphosphorylent alors des sous-unités centrales de l’APC/C, notamment APC1 et APC3.

Ces événements de déphosphorylation permettent le basculement progressif de l’activité de l’APC/C depuis la forme APC/CCdc20 vers APC/CCdh1, assurant la poursuite de la sortie de mitose et la réinitialisation cellulaire.
c. En anaphase B et en télophase, l’action combinée de PP1 et de PP2A orchestre la réinitialisation structurelle de la cellule qui entraîne :
- le désassemblage contrôlé du fuseau mitotique, par la déphosphorylation des MAP et des moteurs mitotiques,
- la stabilisation transitoire de la zone médiane avant sa conversion en corps intermédiaire (midbody).
Parallèlement, la déphosphorylation coordonnée des composants nucléaires favorise :
- la reformation de l'enveloppe nucléaire,
- la décondensation chromosomique,
- la réinstallation progressive de l’architecture interphasique.
3. L'APC/CCdh1 prend progressivement le relais au cours de l’anaphase B et de la télophase, prolongeant l’activité ubiquitine-ligase au-delà de la séparation des chromatides soeurs.
a. Cette extension temporelle de l’ubiquitination élargit le spectre des substrats ciblés et assure l’élimination progressive de régulateurs mitotiques résiduels, notamment :
- Plk1,
- Aurora A (Aurora A’s Functions During Mitotic Exit: The Guess Who Game 2015),
- Aurora B, bien que sa disparition fonctionnelle repose sur une combinaison de mécanismes incluant sa relocalisation vers le corps intermédiaire (midbody), son inactivation enzymatique, la déstabilisation du complexe CPC, puis une ubiquitination dépendante de l’APC/C (Ubiquitin-Mediated Degradation of Aurora Kinases 2016),
- la survivine (BIRC5), dont le devenir est étroitement couplé à celui du complexe CPC, l’inactivation fonctionnelle de ce dernier précédant et conditionnant l’élimination protéolytique de ses composants,
- d’autres facteurs incompatibles avec l’état interphasique, incluant des kinases mitotiques résiduelles, des MAP spécifiques de la mitose, des composants du fuseau et des régulateurs du SAC, dont l’élimination est nécessaire à la réinstallation d’une organisation interphasique stable.
b. L’APC/CCdh1 joue ainsi un rôle central dans le verrouillage durable de la sortie de mitose.
4. L’extinction de l’activité du complexe cycline B/CDK1 (MPF) en anaphase constitue une condition permissive indispensable à l’engagement de la cytokinèse et à l’activation des modules équatoriaux, sans intervenir directement dans les mécanismes effecteurs de la constriction ou de l’abscission.
a. En parallèle, l’extinction progressive de Plk1 est aussi déterminante que son activité préalable.
- Active en amont, Plk1 contribue à l’organisation et à la plasticité des structures mitotiques, mais son maintien empêche la stabilisation durable des structures équatoriales.
- Sa diminution en fin de mitose est donc nécessaire pour permettre la consolidation du fuseau central, la formation du corps intermédiaire (midbody) et l’engagement effectif de la cytokinèse.
b. Plk1 apparaît ainsi comme un régulateur permissif et préparatoire, permettant à la cytokinèse de passer d’un état mitotique dynamique à un état stable compatible avec l’abscission.

La sortie de mitose est un processus activement orchestré par les phosphatases PP1 et PP2A qui imposent une réinitialisation enzymatique globale, transformant un état hautement phosphorylé, mécaniquement contraint et transitoire en une organisation interphasique stable et fonctionnelle.
Retour vers la mitose
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


