Noyau
Lamina nucléaire : dynamique mitotique et fonctions
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

La lamina nucléaire est une structure dynamique dont la polymérisation et la dépolymérisation contrôlent la rupture et la réformation de l’enveloppe nucléaire, tout en assurant l’intégration mécanique et fonctionnelle du noyau.
La dynamique de la lamina nucléaire constitue un mécanisme central du cycle cellulaire, conditionnant l’alternance entre compartimentation nucléaire et accessibilité mitotique des chromosomes par :
- la rupture de l’enveloppe nucléaire, au début de la prométaphase.
- sa reformation en sortie de mitose.
Au-delà de cette plasticité cyclique, la lamina assure en interphase des fonctions mécaniques, organisationnelles et intégratives, reliant architecture nucléaire, organisation du génome et signaux cellulaires.
Lamina et dynamique mitotique
La lamina nucléaire assure, au cours du cycle cellulaire, une transition structurale réversible qui convertit un compartiment nucléaire fermé en une configuration mitotique permissive à la ségrégation des chromosomes (Nuclear envelope remodelling during mitosis 2021).
Rupture de l’enveloppe nucléaire
Au début de la prométaphase, la dépolymérisation des lamines nucléaires entraîne la désintégration de l’enveloppe nucléaire.

Vous pouvez lire : Mitotic dynamics of the nuclear lamina behind the scenes of chromosome separation (2025).
Cette désorganisation ne correspond pas uniquement à une fragmentation membranaire, mais à la levée coordonnée des contraintes structurales exercées par la lamina et les protéines associées sur la chromatine périphérique (Lamina Associated Domains and Gene Regulation in Development and Cancer 2019).
- La dissociation des interactions lamina-chromatine, notamment au niveau des LAD (Lamina-Associated Domains), libère les territoires chromosomiques de leur ancrage périphérique et transforme un compartiment nucléaire fermé en un espace mitotique ouvert.
- Ce processus permet ainsi l’accès des microtubules du fuseau mitotique aux chromosomes condensés, condition indispensable à la ségrégation chromosomique.
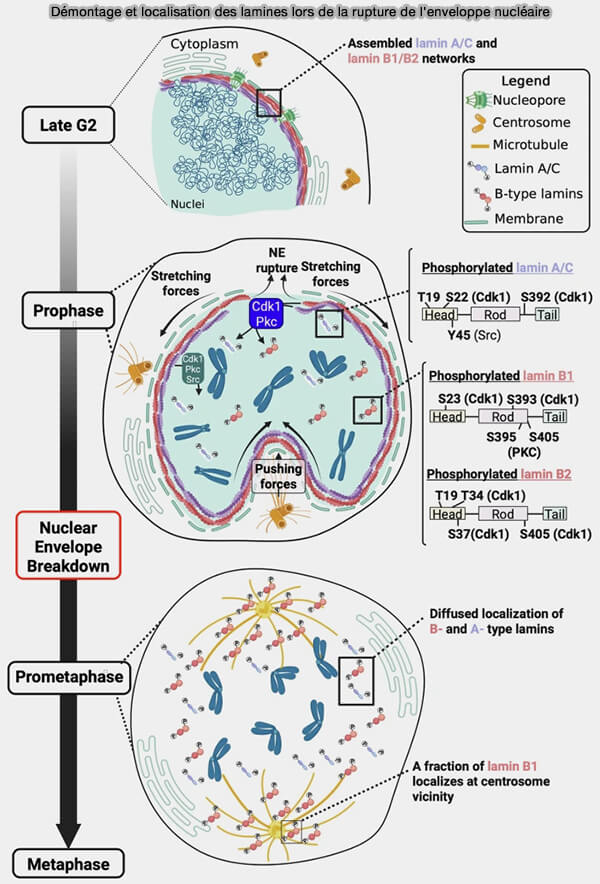
(figure : vetopsy.fr d'après Picotto et col)
1. Ce processus est déclenché par la phosphorylation de résidus sérine spécifiques des trois catégories de lamines (A/C, B1 et B2) par le complexe cycline B/CDK1 (MPF).
La phosphorylation modifie les interactions tête-à-queue et latérales des lamines, empêchant leur polymérisation et conduisant à la dislocation du réseau laminaire sous-jacent à la membrane nucléaire interne.
2. La perte de ce support structural provoque la fragmentation de l’enveloppe nucléaire et la dispersion de ses composants dans le cytoplasme mitotique (Post-Translational Modification of Lamins: Mechanisms and Functions 2022).
a. Les lamines de type B conservent une association transitoire avec des fragments membranaires.
- En raison de leur ancrage lipidique isoprénylique (farnésyl) permanent, les dimères phosphorylés de lamines B restent liés aux membranes dérivées de l’enveloppe nucléaire.
- Cette persistance membranaire permet de maintenir une continuité topologique des membranes nucléaires et prépare leur recrutement rapide autour des masses chromosomiques lors de la télophase, accélérant ainsi la réformation de l’enveloppe nucléaire.
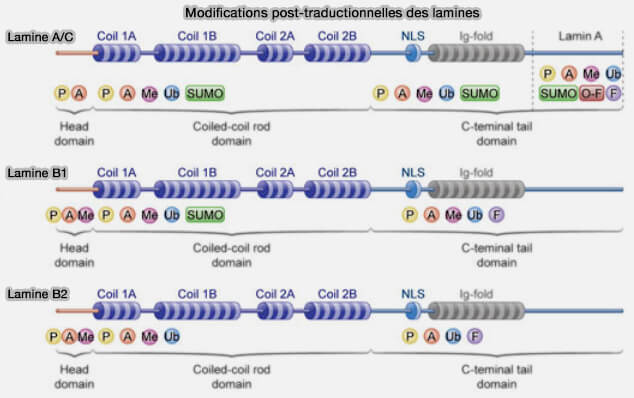
(figure : vetopsy.fr d'après Zheng et col)
b. La lamine A, synthétisée initialement sous forme farnésylée, subit quant à elle un clivage post-traductionnel de son groupe isoprénylique (
- Après la rupture de l’enveloppe nucléaire, elle ne reste associée aux membranes que par des interactions protéine-protéine, notamment avec des protéines de la membrane nucléaire interne telles que les LAP.
- Cette absence d’ancrage lipidique favorise sa redistribution homogène et son réassemblage contrôlé au moment de la reconstitution du noyau interphasique.
3. Parallèlement, plusieurs protéines de la membrane nucléaire interne, LAP, émerine, MAN1 et LBR sont elles-mêmes phosphorylées en entrée de mitose, ce qui diminue leur affinité pour les lamines et pour la chromatine.
La phosphorylation des protéines à domaine LEM et d’adaptateurs comme BAF participe également à la dissociation de la chromatine périphérique, permettant la libération complète des chromosomes dans le cytoplasme mitotique, ce qui entraîne la désorganisation transitoire des territoires chromosomiques, en particulier des LAD (Lamina-Associated Domains).
4. Les pores nucléaires se désintègrent aussi, non pas en protéines isolées, mais en modules structuraux conservés (

La désorganisation ne résulte donc pas uniquement de la dépolymérisation des lamines, mais d’un relâchement global des interactions structurales reliant la lamina, la membrane nucléaire interne et l’hétérochromatine périphérique.
Reformation de l'enveloppe nucléaire
À la fin de l’anaphase et au cours de la télophase, la réformation de l’enveloppe nucléaire est initiée par l’inactivation du complexe cycline B/CDK1 (MPF) et la déphosphorylation progressive des lamines nucléaires par des phosphatases spécifiques, i.e. PP1 et PP2A et ce qui restaure la capacité des lamines à s’assembler et à reformer un réseau polymérique.
La réformation de l’enveloppe nucléaire suit une séquence ordonnée :
- recrutement membranaire initial,
- reconstitution du maillage laminaire périphérique,
- réassemblage des complexes de pores nucléaires,
- stabilisation mécanique et réorganisation de la chromatine.
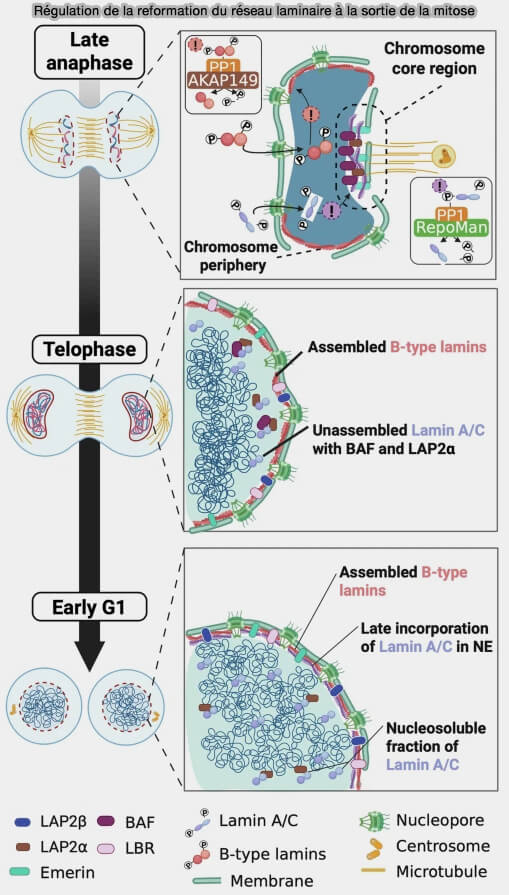
(figure : vetopsy.fr d'après Picotto et col)
1. Les membranes issues de l’enveloppe nucléaire, enrichies en lamines B ancrées par leur groupement farnésyl, sont recrutées à la surface des masses chromosomiques filles.
- Ces membranes s’étalent progressivement autour des chromosomes, amorçant la reconstitution de l’enveloppe nucléaire.
- Les lamines B, du fait de leur ancrage lipidique permanent, constituent le premier échafaudage périphérique, orientant l’enveloppement progressif des chromatides et définissant la future interface nucléaire.
2. Les lamines A/C sont recrutées plus tardivement, principalement après la fermeture quasi complète de l’enveloppe nucléaire.
- Elle s’intègre alors au réseau laminaire en formation par polymérisation et par interactions avec les protéines de la membrane nucléaire interne, contribuant à la maturation mécanique et fonctionnelle du noyau interphasique.
- Ce recrutement différé des lamines A/C renforce secondairement la rigidité et la résistance mécanique du noyau reconstitué.
3. Parallèlement, la déphosphorylation des protéines de la membrane nucléaire interne précédemment phosphorylées (LAP, émerine, MAN1, LBR), ainsi que de l’adaptateur nucléoplasmique BAF, restaure leur affinité pour les lamines et pour la chromatine.
Cette reconstitution progressive de l’interface lamina-membrane-chromatine permet la réassociation des LAD à la périphérie nucléaire et initie la restauration des territoires chromosomiques.
4. La réformation de la lamina accompagne la réorganisation de la chromatine périphérique et la réinsertion des complexes de pores nucléaires, réinstaurant un compartiment nucléaire fermé, mécaniquement stable et spatialement organisé.
Rôles de la lamina
La lamina nucléaire constitue une structure clé de l’architecture nucléaire, assurant l’intégration des propriétés mécaniques, spatiales et fonctionnelles du noyau (
Par son positionnement à l’interface entre enveloppe nucléaire, chromatine et réseaux cytosquelettiques, elle participe à l’intégration de signaux mécaniques ou biochimiques susceptibles d’influencer indirectement l’organisation chromatinienne et les programmes transcriptionnels.

Vous pouvez lire : The nuclear lamina in health and disease (2016).
1. La lamina contribue en premier lieu au maintien de la forme et de la stabilité du noyau.
Par son réseau sous-membranaire, elle renforce mécaniquement l’enveloppe nucléaire et limite les déformations excessives induites par les contraintes internes ou externes.
2. Elle joue également un rôle central dans la connexion du noyau au cytosquelette cytoplasmique, en servant de point d’ancrage à des complexes transmembranaires de l’enveloppe nucléaire (
Ce couplage permet l’intégration du noyau dans la mécanique cellulaire globale et la transmission contrôlée des forces à l’échelle de la cellule.
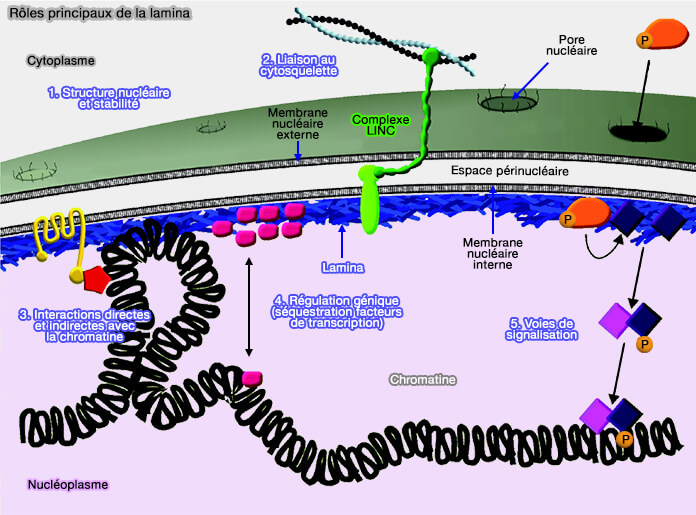
(figure : vetopsy.fr d'après Dittmer)
3. La lamina intervient par ailleurs dans l’organisation spatiale de la chromatine (
En constituant une interface structurée à la périphérie du noyau, elle définit des domaines chromatiniens périphériques et participe à l’ancrage direct ou indirect de régions du génome à l’enveloppe nucléaire, contribuant à la compartimentation fonctionnelle du noyau.
4. Au-delà de cette organisation spatiale, la lamina participe à la régulation de l’expression génique (
Par ses interactions avec des protéines associées à la chromatine et avec certains régulateurs transcriptionnels, elle peut moduler l’accessibilité de régions génomiques ou séquestrer des facteurs de transcription à la périphérie nucléaire, sans agir elle-même comme facteur de transcription.
5. Enfin, la lamina s’inscrit dans des voies de signalisation reliant l’environnement cellulaire aux fonctions nucléaires (

Les lamines sont aussi impliquées dans des maladies génétiques rares appelées laminopathies.
Retour à la structure du noyau
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauEnveloppe nucléairePores nucléairesLaminaCorps nucléairesTransport nucléocytoplasmiqueCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesMicrotubulesReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


