Noyau
Lamina nucléaire : architecture et interfaces structurales
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

La lamina nucléaire est un réseau de lamines et de protéines associées ancré à la membrane nucléaire interne, organisant mécaniquement l’enveloppe et la chromatine périphérique.
(figure : vetopsy.fr)
Structure de
la lamina
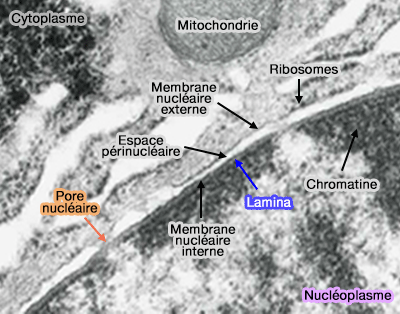
La lamina nucléaire est un réseau protéique dense et hautement organisé, de 10 à 30 nm de large, situé à la face interne de la membrane nucléaire interne qui s'interrompt au niveau des pores nucléaires.
Bien qu’elle soit en continuité avec le nucléoplasme, la lamina constitue un compartiment périphérique spécialisé, assurant une interface structurale et fonctionnelle entre l’enveloppe nucléaire, la chromatine et le nucléosquelette (Proteins that bind A-type lamins: integrating isolated clues 2004).

Vous pouvez lire : The Nuclear Lamina (2022).
Lamines
(figure : vetopsy.fr d'après Alberts)
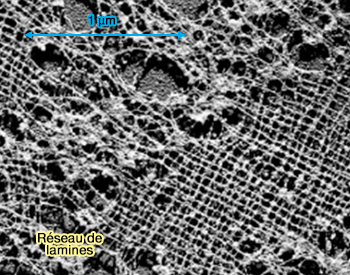
Les lamines A/C et B, issues de gènes distincts, forment le composant structural principal de la lamina.
- Ces protéines s’assemblent par polymérisation pour former un réseau bidimensionnel sous-membranaire qui confère rigidité et résistance mécanique à l'enveloppe nucléaire.
- Les réseaux de lamines A/C et de lamines B forment des maillages partiellement distincts, mais interconnectés, permettant une organisation modulaire de la lamina et une adaptation aux contraintes mécaniques et fonctionnelles du noyau.

Les lamines sont étudiées dans un chapitre spécifique.
Protéines associées aux lamines
Au-delà des lamines elles-mêmes, la lamina comprend un grand nombre de protéines associées, dont la diversité ne cesse d’augmenter.
En 2014, on en recensait environ 54 associées aux lamines de type A/C et 25 aux lamines de type B (Partners and post-translational modifications of nuclear lamins 2013) avec une composition qui varie selon les types cellulaires et les tissus (The nuclear envelope proteome differs notably between tissues 2012).
Les protéines associées à la lamina ne constituent pas une simple liste d’interacteurs, mais se répartissent en grandes classes fonctionnelles qui assurent des rôles complémentaires.
- L’ancrage de la lamina à la membrane nucléaire interne garantit la cohésion mécanique de l’enveloppe nucléaire.
- Le couplage structural entre la lamina et la chromatine permet l’organisation spatiale du génome à la périphérie nucléaire, contribuant à la stabilité des territoires chromosomiques et à la cohérence de l’architecture nucléaire au cours de l’interphase.
- L’intégration de signaux mécaniques et nucléaires conditionne l’adaptation du noyau aux contraintes cellulaires.
L’ensemble de ces interactions permet au noyau de fonctionner comme un compartiment mécaniquement résistant, spatialement organisé et fonctionnellement intégré à la cellule.
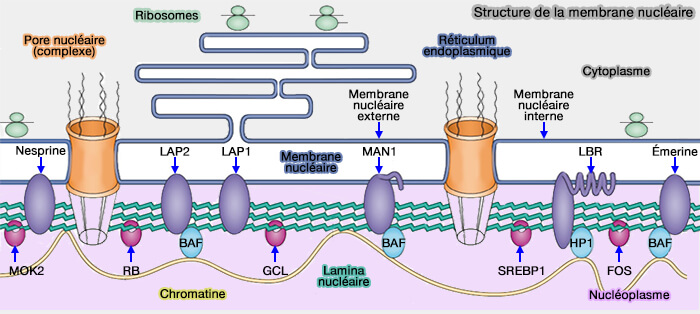
(figure : vetopsy.fr d'après H. D. M Coutinho)
Protéines de la membrane nucléaire interne associées aux lamines
La lamina nucléaire est étroitement connectée à la membrane nucléaire interne par des protéines transmembranaires et périphériques assurant son ancrage et sa stabilité (Lamina-Associated Domains: Links with Chromosome Architecture, Heterochromatin, and Gene Repression 2017).
- Ces protéines forment une interface structurale entre le réseau laminaire, la membrane nucléaire interne et, pour certaines, la chromatine.
- Elles permettent ainsi le maintien mécanique de l’enveloppe nucléaire et l’organisation de la périphérie nucléaire.
1. Parmi ces protéines, plusieurs appartiennent à la famille des protéines à domaine LEM (LEM-D), caractérisées par leur interaction avec BAF et leur rôle d’interface structurale entre la lamina, la membrane nucléaire interne et la chromatine (Networking in the nucleus: A spotlight on LEM-domain proteins 2016).
a. Le domaine LEM (LAP2–Emerin–MAN1) est un motif protéique conservé d’environ 40 acides aminés composé de deux hélices α antiparallèles reliées par une courte boucle et stabilisées par un cœur hydrophobe conservé (Structural analysis of the ternary complex between lamin A/C, BAF and emerin identifies an interface disrupted in autosomal recessive progeroid diseases 2018).
Le domaine LEM se lie à un dimère de BAF, lequel se fixe à l’ADN double brin et peut également interagir avec les lamines, établissant ainsi un pont entre membrane nucléaire interne, lamina et chromatine.
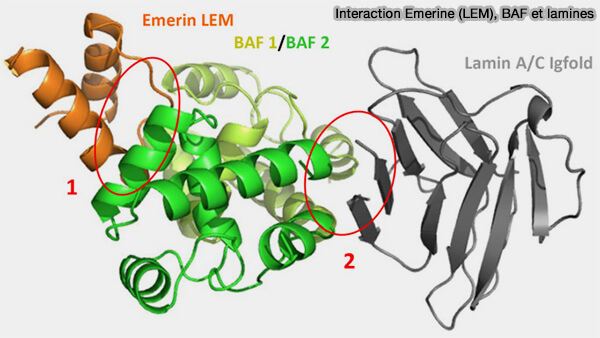
(figure : vetopsy.fr d'après Samson et coll)
b. Les principaux représentants de la membrane nucléaire interne sont LAP2, l’émerine et MAN1, auxquels s’ajoutent d’autres membres humains comme LEMD1, LEMD2 et ANKLE2.
2. Les protéines LAP1 et LAP2 (Lamin-Associated Proteins) forment une famille de protéines associées aux lamines, localisées à la membrane nucléaire interne.
- Elles interagissent principalement avec les lamines A/C et participent à la stabilisation de la lamina contre la membrane.
- Certaines isoformes de LAP2, notamment LAP2β, appartiennent aux protéines à domaine LEM et assurent également des interactions avec la chromatine, renforçant le lien structurel entre lamina et génome périphérique.
Remarque : le terme Lamin-Associated Proteins (LAP) désigne spécifiquement la famille comprenant LAP1 et LAP2 (et leurs isoformes) et ne doit pas être confondu avec l’ensemble plus large des protéines associées aux lamines, qui inclut notamment les protéines à domaine LEM, LBR ou d’autres partenaires structuraux et régulateurs.
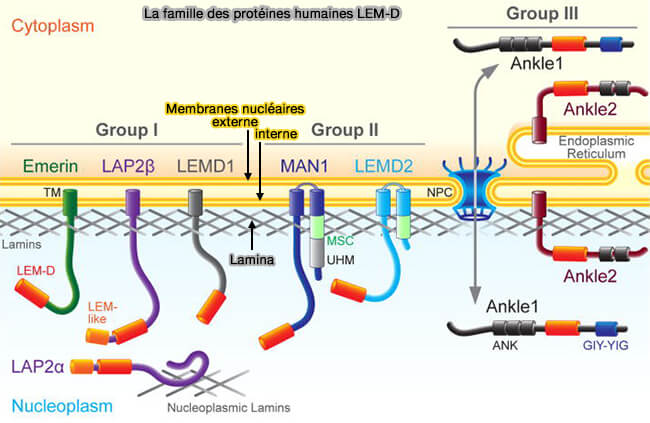
(figure : vetopsy.fr d'après Barton et coll)
3. L'émerine, protéine à domaine LEM, est une protéine intégrale de la membrane nucléaire interne fortement associée aux lamines A/C.
a. Elle établit des contacts avec (The Role of Emerin in Cancer Progression and Metastasis 2021) :
- des régulateurs de la transcription et de la maturation des ARNm,
- la protéine BAF (The molecular basis of emerin–emerin and emerin–BAF interactions 2015 et Structural analysis of the ternary complex between lamin A/C, BAF and emerin identifies an interface disrupted in autosomal recessive progeroid diseases 2018).
- plusieurs protéines de l’enveloppe nucléaire, notamment LAP2 ou MAN1.
b. Par ces interactions, l’émerine renforce la cohésion mécanique de l’enveloppe nucléaire et la résistance du noyau aux contraintes physiques (Lamin A/C and Emerin depletion impacts chromatin organization and dynamics in the interphase nucleus 2019).
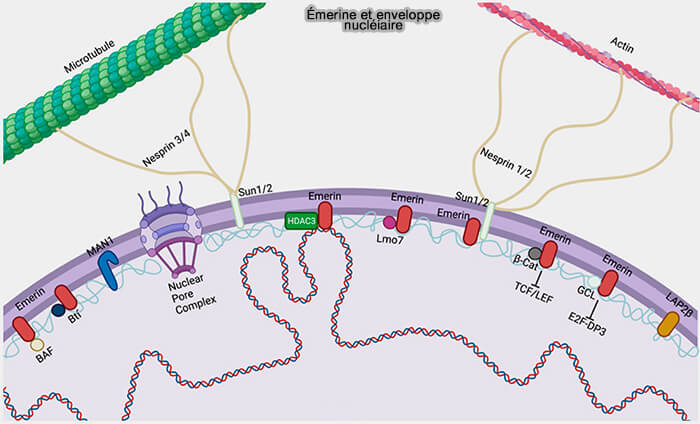
(figure : vetopsy.fr d'après Liddane et Holaska)
4. MAN1 (LEM domain-containing protein 3) est une protéine à domaine LEM de la membrane nucléaire interne, impliquée dans l’ancrage de la lamina et l’organisation de l’enveloppe nucléaire.
45 LBR (Lamin B Receptor) est une protéine transmembranaire de la membrane nucléaire interne associée aux lamines de type B (Lamin B receptor 2010).
a. LBR établit des interactions avec :
- les lamines B, assurant leur ancrage stable à la membrane nucléaire interne,
- l’ADN et les histones,
- des protéines associées à la chromatine, notamment HP1, impliquée dans l’organisation de l’hétérochromatine périphérique.
b. Par ces interactions, LBR participe à l’ancrage et à l’organisation de l’hétérochromatine à la périphérie du noyau, assurant la continuité structurale entre la lamina B, la membrane nucléaire interne et la chromatine sous-jacente.
Protéines de liaison entre la lamina et la chromatine
La lamina nucléaire est reliée à la chromatine périphérique par des protéines adaptatrices.
1. BAF (Barrier-to-Autointegration Factor) est une petite protéine hautement conservée capable de se lier à l’ADN double brin, aux histones et aux lamines (The molecular basis of emerin–emerin and emerin–BAF interactions 2014).
Elle agit comme un pont entre la lamina, la chromatine et les protéines à domaine LEM (LAP2, MAN1, émerine), assurant l’ancrage de la chromatine périphérique et la reconnexion lamina–chromatine en sortie de mitose.
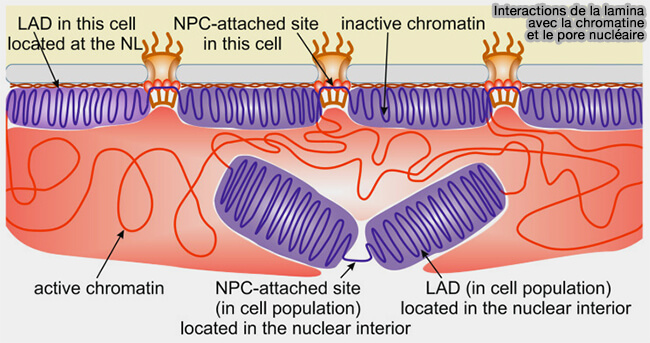
(Figure : vetopsy.fr d'après Shevelyov)
2. HP1 (Heterochromatin Protein 1) HP1 est une protéine associée à l’hétérochromatine, impliquée dans la reconnaissance et le maintien de domaines chromatiniens condensés.
- Elle interagit indirectement avec la lamina nucléaire, notamment par l’intermédiaire de protéines de la membrane nucléaire interne telles que LBR, et contribue à l’ancrage de l’hétérochromatine à la périphérie nucléaire.
3. Certaines protéines de la membrane nucléaire interne, telles que LAP2β et LBR, déjà impliquées dans l’ancrage de la lamina, assurent la liaison à la chromatine, constituant une interface directe entre membrane nucléaire interne, réseau laminaire et génome.
Partenaires régulateurs et fonctionnels de la lamina
La lamina agit aussi comme une plateforme d’intégration de signaux cellulaires, sans régulation directe.
1. Certaines protéines clés du contrôle du cycle cellulaire interagissent avec la lamina, illustrant son implication indirecte dans la coordination entre architecture nucléaire et prolifération.
Rb (RetinoBlastoma transcriptional regulator) interagit avec la lamina nucléaire, contribuant à l’organisation spatiale du contrôle du cycle cellulaire.
2. Des protéines impliquées dans la différenciation cellulaire et la spécialisation tissulaire interagissent également avec la lamina.
- GCL (Germ Cell-Less) agit comme répresseur transcriptionnel, par exemple en maintenant réprimés des gènes de différenciation somatique dans les cellules germinales.
- MOK2 module l’expression de gènes spécifiques en se liant à l’ADN ou aux ARN, notamment dans des programmes de différenciation neuronale.
L’association de ces protéines à la lamina permet de restreindre leur accès à certaines régions du génome, conditionnant leur activité selon l’état de différenciation cellulaire, sans régulation transcriptionnelle directe par la lamina.
3. Des régulateurs métaboliques et des facteurs sensibles à l’environnement cellulaire peuvent aussi interagir avec la lamina (Role of lamins in 3D genome organization and global gene expression 2019).
- SREBP1 (Sterol Response Element Binding Protein 1), facteur impliqué dans la régulation du métabolisme lipidique, a été décrit comme pouvant interagir avec des composants de la lamina, illustrant le lien entre organisation nucléaire et signaux métaboliques (
régulation des lipides).
- Des facteurs comme FOS, impliqués dans les réponses transcriptionnelles rapides à des signaux extracellulaires (facteurs de croissance, stress), peuvent être transitoirement associés à la périphérie nucléaire, suggérant un rôle de la lamina dans leur disponibilité spatiale avant ou après activation.
Ces interactions multiples confèrent à la lamina un rôle central dans l’architecture nucléaire, la compartimentation de la chromatine et la coordination entre structure nucléaire et fonctions cellulaires.
Dynamique mitotique et fonctions de la lamina
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauEnveloppe nucléairePores nucléairesLaminaCorps nucléairesTransport nucléocytoplasmiqueCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesMicrotubulesReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


