Corps nucléaires
Organisation fonctionnelle et dynamique
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

Les corps nucléaires sont des compartiments non membranaires dynamiques organisant spatialement la transcription, la maturation des ARN et la réponse cellulaire au stress.
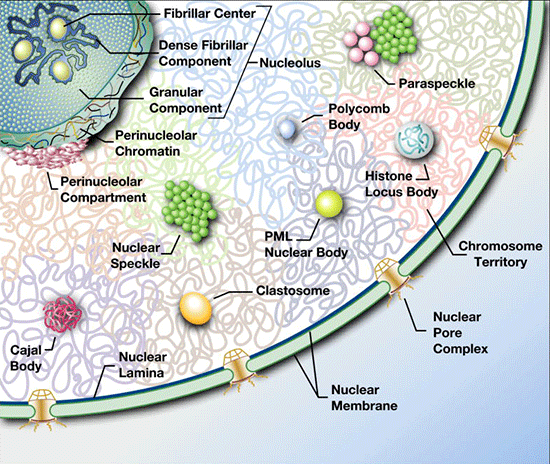
(Figure : avec l'aimable autorisation de David Spector)
Vue d'ensemble
1. Les corps nucléaires sont des compartiments intranucléaires non membranaires correspondant à des condensats biomoléculaires enrichis en protéines et en ARN, organisés dynamiquement au sein du nucléoplasme.

Les condensats biomoléculaires par séparation de phase liquide-liquide permettent la création de micro-environnements réactionnels spécialisés, favorisant certaines réactions biologiques sans compartimentation membranaire.
2. Du point de vue structural, un corps nucléaire se définit par :
- une composition moléculaire enrichie mais non exclusive, comme l’enrichissement en protéines PML et partenaires associés dans les PML bodies,
- une frontière diffuse résultant d’un gradient de concentration (
condensats)
- une dynamique d’échange rapide avec le nucléoplasme environnant,
- une dépendance à l’état transcriptionnel et métabolique de la cellule, comme l’augmentation de taille du nucléole lors d’une activité ribosomique accrue.
3. Du point de vue fonctionnel, les corps nucléaires constituent des micro-domaines régulés dont l’assemblage et la stabilité dépendent :
- de la concentration locale de ses composants, comme l’augmentation de protéines d’épissage favorisant l’expansion des speckles,
- de la présence d’ARN structurants, par exemple le lncRNA NEAT1 indispensable à la formation des paraspeckles,
- des modifications post-traductionnelles des protéines d'échafaudage, comme la SUMOylation régulant la stabilité des PML bodies,
- de l’état global du noyau au cours du cycle cellulaire, illustré par la dissolution de nombreux corps nucléaires lors de la mitose.
Les corps nucléaires représentent des unités organisationnelles intermédiaires entre la chromatine structurée et le nucléoplasme diffus, assurant une compartimentation fonctionnelle fine au sein du noyau sans recourir à une membrane.
Logique fonctionnelle des corps nucléaires
Les corps nucléaires organisent spatialement des processus moléculaires qui seraient moins efficaces s’ils étaient diffus dans le nucléoplasme et forment des micro-domaines régulés essentiels à la structuration fonctionnelle du noyau.
Leur fonctionnement repose sur quatre principes fonctionnels majeurs qui structurent leur activité et constituent le cadre d’interprétation moderne des corps nucléaires, indépendamment de leur morphologie apparente (Biogenesis and function of nuclear bodies 2011).
1. Les corps nucléaires concentrent enzymes, substrats et cofacteurs dans un volume restreint, augmentant la probabilité d’interactions productives et améliorant la cinétique et la spécificité des réactions.
Le nucléole illustre ce principe par la transcription et la maturation coordonnées des ARN ribosomiques (ARNr).
2. Ils constituent des hubs d’interaction où convergent protéines régulatrices, ARN et complexes enzymatiques, permettant la coordination de voies moléculaires distinctes et le couplage transcription–épissage.
Les speckles regroupent ainsi des facteurs d’épissage au voisinage des gènes activement transcrits.
3. Certains compartiments exercent une fonction de séquestration transitoire, modulant la disponibilité de facteurs de transcription ou de transcrits nucléaires et régulant ainsi leur activité ou leur export.
Les paraspeckles retiennent par exemple certains ARN messagers contenant des éléments répétitifs Alu dans leur région 3′ non traduite dans le noyau, modulant leur disponibilité cytoplasmique.
4. De nombreux corps nucléaires présentent une plasticité marquée, apparaissant, disparaissant ou se remodelant en réponse à l’activité transcriptionnelle, au cycle cellulaire ou aux stress cellulaires.
Les nuclear stress bodies illustrent cette capacité d’adaptation rapide du noyau.
Formation et régulation des condensats nucléaires
L’assemblage des corps nucléaires repose majoritairement sur la formation de condensats biomoléculaires issus d’interactions multivalentes entre protéines et ARN au sein du nucléoplasme, selon des principes physico-chimiques (
Contrairement aux organites membranaires, leur formation ne dépend pas d’un bourgeonnement ou d’un cloisonnement lipidique, mais d’une transition locale d’état physico-chimique, conduisant à une séparation de phase liquide-liquide et/ou à l’établissement de réseaux coopératifs dynamiques pouvant évoluer vers des états viscoélastiques intermédiaires.
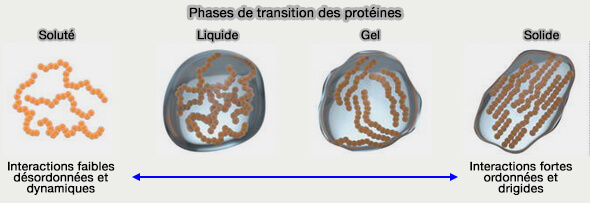
(Figure : vetopsy.fr d'après Boeynaems et coll)
1. Des protéines possédant des domaines intrinsèquement désordonnés (IDR), des répétitions modulaires ou des régions riches en résidus chargés établissent des interactions faibles mais coopératives.
a. Lorsque la concentration critique est atteinte, ces interactions peuvent déclencher une séparation de phase générant un compartiment dynamique dont la composition reste modulable.
b. Ce modèle rend compte :
- de la fusion possible de deux corps voisins, comme pour les speckles,
- de leur sensibilité aux variations de concentration,
- de leur dissolution ou de leur reconfiguration lors de la mitose, notamment en raison des phosphorylations massives dépendantes des kinases mitotiques, ou lors de stress cellulaires modifiant l’environnement physico-chimique nucléaire.
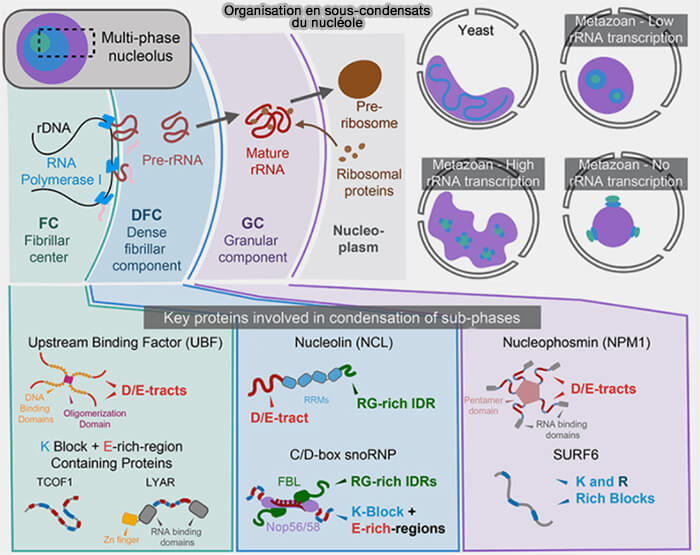
(Figure : vetopsy.fr d'après King et coll)
2. L’assemblage du condensat peut être initié par un élément nucléateur spécifique et est ensuite modulé par plusieurs facteurs régulateurs.
a. La nucléation peut dépendre :
- d’un ARN long non codant, par exemple NEAT1 des paraspeckles, ou les transcrits Sat III dans les nuclear stress bodies,
- d’une protéine organisatrice multivalente, comme PML dans les PML bodies, capable de recruter par interactions SUMO-dépendantes de multiples partenaires,
- d’un locus chromatinien actif servant de point d’ancrage initial, par exemple un locus d’ADNr dans le nucléole.
b. L’assemblage est ensuite modulé par :
- des modifications post-traductionnelles, phosphorylation, SUMOylation, ubiquitination et acétylation,
- des variations de concentration des composants,
- la transcription locale et la dynamique des ARN associés, qui peuvent stabiliser ou remodeler le condensat,
- le cycle cellulaire.
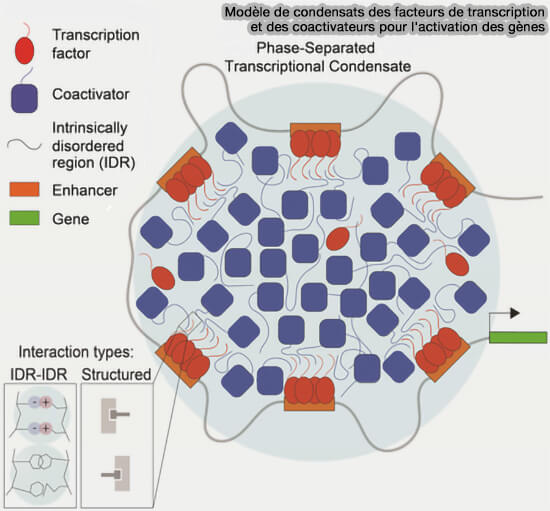
(Figure : vetopsy.fr d'après Boijja et coll)
Classification fonctionnelle des corps nucléaires
Les corps nucléaires ne sont plus classés principalement selon leur morphologie, mais selon leur fonction biologique dominante et leur organisation moléculaire, reflétant ainsi la diversité des processus nucléaires qu’ils compartimentent.
1. Les corps liés à la biogenèse des ARN regroupent des structures qui concentrent les facteurs nécessaires à la synthèse, à la maturation et à l’assemblage des ribonucléoprotéines.
Ils participent notamment à la transcription et à la maturation des ARN ribosomiques, à la modification et à l’assemblage des snARN, ainsi qu’à la maturation des ARN d’histones.
- 1.1 Le nucléole constitue le compartiment central de la transcription des ARN ribosomiques (ARNr) et de l’assemblage des sous-unités ribosomiques.
- 1.2 Les corps de Cajal participent à la maturation et à l’assemblage des snRNP et de certaines ribonucléoprotéines spécialisées.
- 1.3 Les histone locus bodies sont impliqués dans la régulation transcriptionnelle et la maturation spécifique des ARNm d’histones.
2. Les corps liés à la régulation transcriptionnelle regroupent des domaines qui organisent la distribution spatiale des facteurs de transcription et des complexes de régulation co-transcriptionnelle.
Ils interviennent dans la régulation fine de l’expression génique, dans l’organisation des domaines transcriptionnellement actifs et dans la coordination entre transcription et épissage.
2.1 Les corps impliqués dans la maturation co-transcriptionnelle des pré-ARNm, qui concentrent des facteurs d’épissage et de traitement des transcrits naissants (pré-ARNm), comprennent :
- les speckles (grains interchromatiniens),
- les cleavage bodies,
- les Sam68 bodies,
- les domaines OPT.
2.2 Les corps ARN-dépendants de séquestration, représentés par les paraspeckles, permettent la rétention nucléaire de certains ARN, la modulation de leur disponibilité cytoplasmique et l’adaptation transcriptionnelle contextuelle.
2.3 Les corps liés à l’organisation de la chromatine participent à l’organisation de la chromatine et au contrôle spatial de l’expression génique, tels que :
- les Polycomb bodies,
- les PML bodies,
- le compartiment périnucléolaire,
2.4 Les corps induits par le stress et la dégradation protéique regroupent des compartiments transitoires qui se forment ou se remodèlent en réponse à des contraintes cellulaires, tels que :
- les nuclear stress bodies, qui apparaissent lors de stress cellulaires et participent à la reprogrammation transcriptionnelle,
- les clastosomes, domaines nucléaires enrichis en protéasomes impliqués dans la dégradation de protéines nucléaires ubiquitinées (
dégradation protéasomale)
Plasticité et reprogrammation des corps nucléaires
Les corps nucléaires sont des condensats dynamiques dont la formation, la taille et la composition varient en fonction du contexte cellulaire.
1. Leur plasticité s’exprime au cours :
- du cycle cellulaire,
- de la différenciation cellulaire,
- des variations métaboliques,
- des stress environnementaux,
- de la transformation tumorale ou d’infections virales.
2. Certains compartiments sont constitutifs (nucléole, speckles), tandis que d’autres apparaissent ou se remodèlent transitoirement (nuclear stress bodies, clastosomes), illustrant la capacité du noyau à reconfigurer rapidement son organisation fonctionnelle.
Dysfonctionnement et pathologies
Des altérations de la formation, de la stabilité ou de la régulation des corps nucléaires sont associées à diverses pathologies.
1. Ces dérégulations peuvent concerner :
- l’oncogenèse, par exemple la désorganisation des PML bodies dans certaines leucémies aiguës promyélocytaires (LAP) ou la dérégulation des Polycomb bodies dans des cancers associés à une répression épigénétique aberrante,
- les maladies neurodégénératives, telles que la sclérose latérale amyotrophique (SLA) ou certaines démences frontotemporales, caractérisées par des agrégats ribonucléoprotéiques anormaux affectant des protéines associées aux speckles ou aux paraspeckles,
- les défauts de maturation des ARN et les dysfonctions de l’épissage, observés dans certaines myélodysplasies ou dans l’amyotrophie spinale liée à des anomalies des corps de Cajal,
- les perturbations de la SUMOylation, qui modulent la stabilité des PML bodies et peuvent contribuer à des syndromes tumoraux ou à des troubles de la réponse au stress,
- les anomalies de la réponse aux dommages de l’ADN, impliquant des foyers nucléaires spécialisés et affectant la surveillance de l’intégrité génomique.
2. Les défauts d’assemblage ou de désassemblage des condensats nucléaires peuvent ainsi altérer l’organisation spatiale du noyau, perturber l’expression génique globale et compromettre l’homéostasie cellulaire.
Retour au noyau
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauEnveloppe nucléairePores nucléairesLaminaCorps nucléairesTransport nucléocytoplasmiqueCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesMicrotubulesReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


