Corps nucléaires
Corps liés à la régulation transcriptionnelle
2.4. Corps induits par le stress et la dégradation protéique
Nuclear stress body et clastosomes
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

Les nuclear stress bodies et les clastosomes sont des compartiments nucléaires transitoires induits par le stress, respectivement organisés autour d’ARN répétitifs Sat III et de protéasomes nucléaires concentrés.
Nuclear Stress Body
Les nuclear stress bodies (nSB) sont des compartiments nucléaires irréguliers, de 0,3 à 3 μm de diamètre, généralement présents au nombre de 2 à 10 par noyau, qui se forment en réponse à un stress cellulaire aigu (Nuclear Stress Bodies 2010).
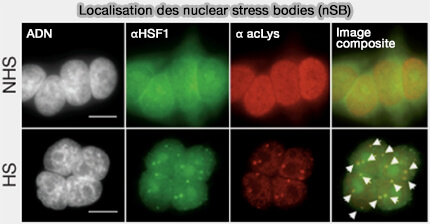
(Figure : vetopsy.fr d'après Biamonti et Vourc’h)
1. Les nSB ne sont pas des sites de transcription classique de gènes codants, mais des compartiments nucléaires spécialisés organisés autour d’ARN répétés et formés lors de stress cellulaires, notamment thermique, oxydatif ou toxique, par activation du facteur de transcription HSF1 (Heat Shock Factor 1).
Cette appellation " choc thermique " est un terme historique qui s'applique à tous les types de stress et non pas seulement à la chaleur.
2. HSF1 activé se lie directement aux séquences répétées satellite III situées dans les régions péricentromériques du génome, en particulier sur le chromosome 9 chez l’humain (Heat Shock Factor 1 forms nuclear condensates and restructures the yeast genome before activating target genes 2024).
- Les séquences satellite III sont des régions d’ADN répétitif péricentromérique normalement silencieuses, qui deviennent transcrites en ARN non codants lors d’un stress cellulaire et servent de support à la formation des nuclear stress bodies (Heat Shock Factor 1 forms nuclear condensates and restructures the yeast genome before activating target genes 2024).
- Le chromosome 9 possède la plus grande concentration de répétitions Sat III, ce qui en fait le principal site de formation des nSB chez l’humain.
3. La transcription des séquences satellite III conduit à l’accumulation locale d’ARN Sat III qui forment le cœur structurant du nSB (Nuclear stress bodies: a potential mechanism to shut off lethal inflammatory cytokines 2025).
- Ces ARN servent de plateforme moléculaire pour le recrutement progressif de nombreuses protéines, notamment HSF1 lui-même, des facteurs d’épissage et des protéines de liaison à l’ARN telles que SAFB, conduisant à une organisation concentrique et dynamique du compartiment.
- L’ajustement de réseaux transcriptionnels liés à la réponse au stress, inclut certains gènes impliqués dans la régulation inflammatoire, tels que NFIL3 (Nuclear Factor, Interleukin 3 Regulated), un facteur de transcription qui module l’expression de cytokines et participe au contrôle de la réponse inflammatoire excessive.
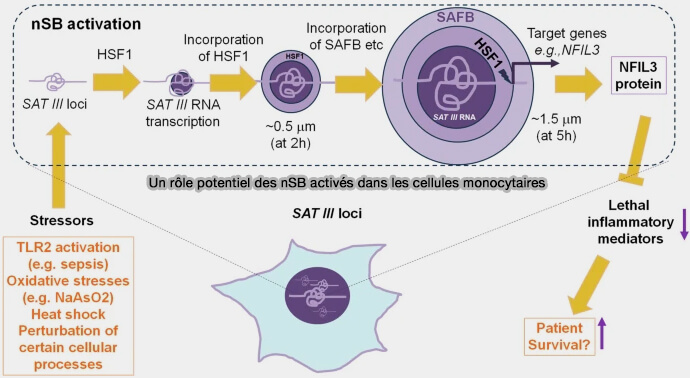
(Figure : vetoppsy.fr d'après Kim)
4. Les nuclear stress bodies participent à une reprogrammation rapide, transitoire et globale de l’expression génique lors d’un stress cellulaire, tout en contribuant au maintien de l’intégrité du génome, notamment par :
- un remodelage local de la chromatine au niveau des régions péricentromériques,
- la séquestration transitoire de certains facteurs de transcription et de protéines d’épissage,
- la modulation de l’épissage alternatif de nombreux transcrits.
Clastosomes
Les clastosomes sont des compartiments nucléaires transitoires irréguliers, de 0,2–1,2 μm de diamètre et généralement présents en nombre limité (0 à 3 par noyau) qui apparaissent dans des cellules présentant une activité transcriptionnelle élevée ou une accumulation accrue de protéines nucléaires ubiquitinées (Clastosome: A Subtype of Nuclear Body Enriched in 19S and 20S Proteasomes, Ubiquitin, and Protein Substrates of Proteasome 2002 et Orphan Nuclear Bodies 2010).
Ils représentent des micro-domaines nucléaires fonctionnels couplant activité transcriptionnelle et contrôle protéostatique.
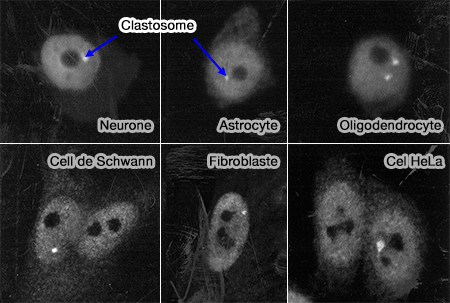
(Figure : vetopsy.fr d'après Lafarga)
1. Contrairement aux nuclear stress bodies, les clastosomes ne sont pas organisés autour d’ARN répétés, mais correspondent à des zones nucléaires spécialisées dédiées à la dégradation protéique dépendante du protéasome, où le protéasome 26S (complexe 20S catalytique associé au complexe 19S régulateur) est localement concentré et actif.
a. Leur formation est favorisée par :
- une stimulation transcriptionnelle intense,
- une augmentation de protéines mal conformées ou régulatrices à demi-vie courte,
- certains stress cellulaires affectant l’homéostasie protéique.
b. Le protéasome 26S est majoritairement assemblé dans le cytoplasme, puis importé dans le noyau via des signaux de localisation nucléaire (NLS) et les clastosomes ne correspondent pas à un assemblage de novo, mais à une concentration locale et transitoire de protéasomes nucléaires recrutés par une accumulation de substrats polyubiquitinés.
b. Ils peuvent apparaître dans des cellules du système nerveux ou dans des contextes de forte activité protéasomale nucléaire.
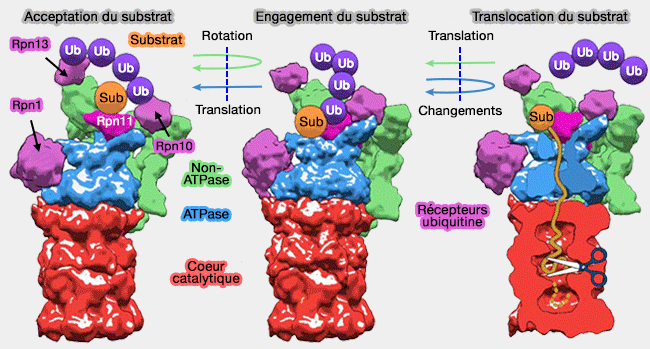
(Figure : vetopsy.fr d'après Unverdorben)
3. Les clastosomes participent à la régulation fine de l’expression génique en assurant la dégradation rapide :
- de facteurs de transcription activés tels que p53, c-Jun ou c-Fos,
- de co-activateurs ou co-répresseurs comme SRC-3, co-activateur stéroïdien,
- des protéines nucléaires ubiquitinées impliquées dans la réponse au stress, notamment IκBα après activation NF-κB.
Remarque : les clastosomes ont été décrits comme pouvant, dans certains contextes, être associés à des sous-populations de PML bodies enrichies en protéasome.
Extensions aux domaines nucléaires induits par le stress
Les nuclear stress bodies et les clastosomes illustrent deux modalités distinctes de compartimentation nucléaire induite par le stress, respectivement ARN-dépendante et protéasome-dépendante.
1. D’autres structures nucléaires transitoires peuvent apparaître dans des contextes de stress, notamment les foyers de réponse aux dommages de l'ADN tels que :
- les 53BP1 bodies (Around and beyond 53BP1 Nuclear Bodies 2017),
- les domaines enrichis en γH2AX (Double strand break repair functions of histone H2AX 2013).
H2AX est une variante de l’histone H2A incorporée dans les nucléosomes, caractérisée par une extension C-terminale spécifique contenant le motif SQ(E/D), permettant sa phosphorylation (γH2AX) sur la sérine 139 lors des cassures double brin de l’ADN.
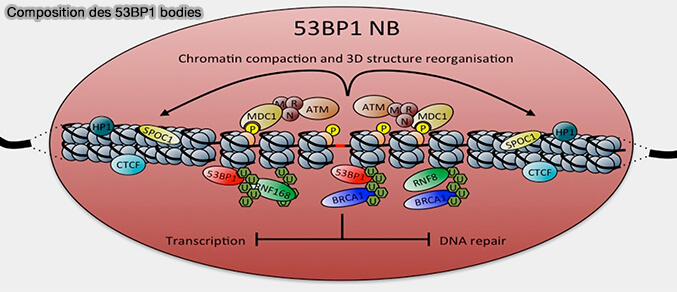
(Figure : vetopsy.fr d'après Fernandez-Vidal et coll)
2. Ces domaines correspondent à des sites localisés de signalisation et de réparation ancrés à la chromatine lésée et ne constituent pas des corps nucléaires autonomes, mais des micro-domaines fonctionnels directement associés à l’ADN endommagé.
Retour à la classification des corps nucléaires
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauEnveloppe nucléairePores nucléairesLaminaCorps nucléairesTransport nucléocytoplasmiqueCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesMicrotubulesReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


