Noyau
Pores nucléaires : organisation fonctionnelle et dynamique
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

Les pores nucléaires associent une barrière sélective centrale, des extensions périphériques et des interactions avec la lamina nucléaire, assurant la régulation dynamique des échanges nucléocytoplasmiques.
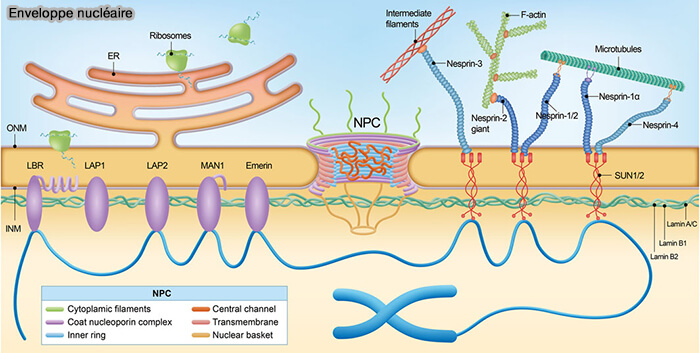
(Figure : vetopsy.fr d'après Wu et coll)
Après avoir décrit l’architecture du pore nucléaire, i.e. charpente protéique organisée en anneau interne et anneaux externes, ancrée dans l’enveloppe nucléaire par des nucléoporines transmembranaires, il convient d’examiner son organisation fonctionnelle (
Si la charpente annulaire ancrée dans la membrane constitue le support structural du pore, sa sélectivité repose sur ses éléments centraux et périphériques :
- la barrière sélective formée par les nucléoporines FG,
- les extensions cytoplasmiques et le panier nucléaire du pore.
Nous aborderons ensuite :
Barrière sélective du canal central
Nucléoporines FG
Les nucléoporines FG constituent la phase centrale du NPC responsable de la sélectivité du transport nucléocytoplasmique et sont enrichies en répétitions courtes contenant une phénylalanine (F) suivie d’une glycine (G), souvent sous les formes FG, GLFG ou FxFG.
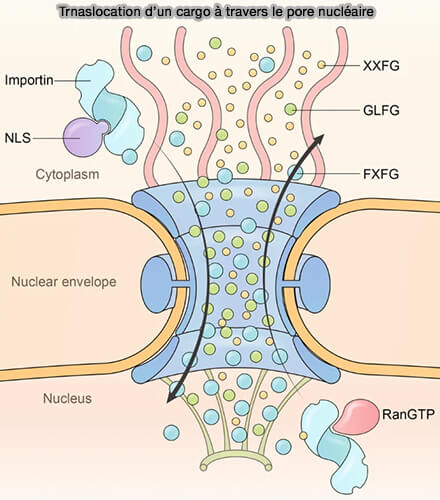
(Figure : vetopsy.fr d'après Yang et coll)
1. Les domaines FG sont majoritairement intrinsèquement désordonnés et s’étendent vers l’intérieur du canal central, où ils forment un réseau dynamique de chaînes flexibles.
Ce réseau occupe l’espace du canal et établit une barrière perméable aux petites molécules diffusibles, mais restrictive pour les macromolécules dépourvues de récepteurs de transport.
2. La sélectivité repose sur des interactions multivalentes et transitoires entre motifs FG et karyophérines (importines/exportines).
La barrière FG n’est pas un " bouchon " statique, mais une matrice polymérique mobile dont les propriétés physiques (densité, cohésion, dynamique) conditionnent la perméabilité du canal.
Remarque : certaines nucléoporines FG participent également aux filaments cytoplasmiques et au panier nucléaire, où elles contribuent aux interactions transitoires avec les karyophérines en amont (capture/docking) et en aval (sortie/libération) de la traversée (
Modèles physiques de la barrière FG
La nature intrinsèquement désordonnée des nucléoporines FG a conduit à plusieurs modèles visant à expliquer comment le canal central peut être à la fois perméable et hautement sélectif.
Quel que soit le modèle retenu, plusieurs principes sont constants (The selective permeability barrier in the nuclear pore complex 2016) :
- les domaines FG sont intrinsèquement désordonnés,
- les interactions sont faibles, multivalentes et réversibles,
- la sélectivité repose sur la reconnaissance spécifique des motifs FG par les karyophérines, et la barrière demeure dynamique plutôt que rigide.
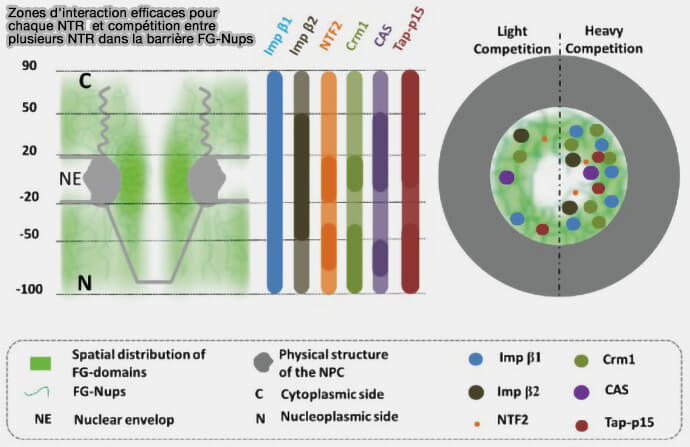
(Figure : vetopsy.fr d'après Li et coll)
1. Le modèle du gel sélectif (hydrogel cohésif) propose que les répétitions FG interagissent entre elles par des contacts hydrophobes faibles mais nombreux, formant un réseau cohésif tridimensionnel comparable à un hydrogel (A Saturated FG-Repeat Hydrogel Can Reproduce the Permeability Properties of Nuclear Pore Complexes 2007 et FG/FxFG as well as GLFG repeats form a selective permeability barrier with self-healing properties 2009)
a. Dans cette configuration :
- les petites molécules diffusent librement.
- les macromolécules non reconnues sont exclues.
- les complexes karyophérine–cargo traversent le réseau en établissant des interactions transitoires et multivalentes avec les motifs FG, ce qui induit une dissolution locale et réversible de la cohésion.
b. La sélectivité repose donc sur une cohésion contrôlée du réseau FG.
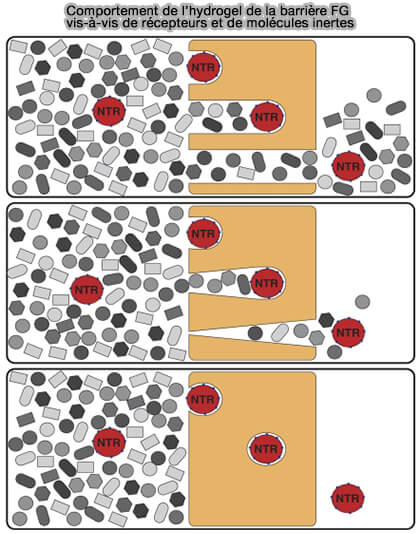
(Figure : vetopsy.fr d'après Frey et Görlich)
2. Dans le modèle de la brosse polymérique, les domaines FG sont considérés comme des chaînes polymériques flexibles ancrées à la paroi du canal (A physical model describing the interaction of nuclear transport receptors with FG nucleoporin domain assemblies 2016).
a. Les chaînes occupent l’espace par entropie.
- Elles génèrent une barrière entropique qui défavorise l’entrée des macromolécules volumineuses non spécifiques.
- Les récepteurs de transport peuvent progresser en établissant des interactions successives avec les chaînes.
b. Ici, la sélectivité repose davantage sur la dynamique des chaînes que sur une cohésion de type gel.
3. Des travaux plus récents suggèrent que les nucléoporines FG peuvent présenter des propriétés de séparation de phase liquide–liquide (The liquid state of FG-nucleoporins mimics permeability barrier properties of nuclear pore complexes 2019).
a. Dans cette perspective, elles formeraient une phase condensée enrichie en FG au centre du pore,
- Cette phase serait dynamique, réversible et modulable.
- Les karyophérines, grâce à leurs surfaces multivalentes de liaison aux FG, seraient capables de partitionner sélectivement dans cette phase.
b. Ces modèles hybrides combinent cohésion locale, désordre intrinsèque et dynamique de phase.
Extensions périphériques
Les extensions périphériques du NPC prolongent sa fonction au-delà du simple canal central.
Filaments cytoplasmiques
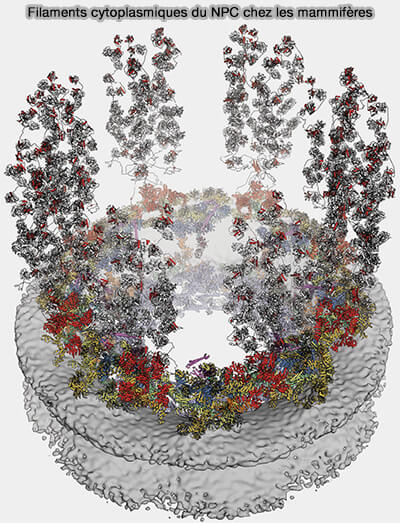
(Figure : vetopsy.fr d'après Bley et coll)
Les filaments cytoplasmiques, assemblage multiprotéique appelé CFNC (Cytoplasmic Filament Nup Complex) constituent des prolongements flexibles du pore nucléaire orientés vers le cytosol (Architecture of the cytoplasmic face of the nuclear pore 2022).
- Ils sont au nombre de huit, disposés selon la symétrie octogonale du pore et ancrés aux unités répétitives de l’anneau cytoplasmique.
- Ces filaments sont formés de nucléoporines spécifiques, dont plusieurs comportent des répétitions FG, ce qui leur permet d’interagir transitoirement avec les karyophérines.
Panier nucléaire
Le panier nucléaire constitue l’extension périphérique du NPC du côté nucléoplasmique (The molecular architecture of the nuclear basket 2024).
1. Le panier adopte une architecture en forme de cage ouverte.
- Il est composé de huit filaments, disposés selon la symétrie octogonale du por.
- Les filaments du panier nucléaire, majoritairement constitués de TPR, émergent de l’anneau nucléaire, convergent vers l’axe central et sont reliés par un anneau distal terminal dont la composition moléculaire précise n’est pas résolue chez les mammifères.
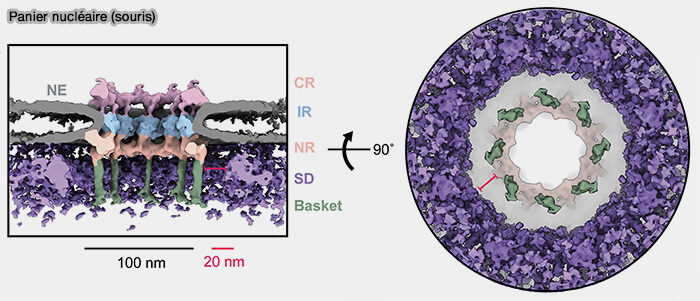
(Figure : vetopsy.fr d'après Singh et coll)
2. Cette organisation tridimensionnelle crée un espace structuré à la sortie nucléaire du canal central qui ne participe pas directement au filtrage FG du canal.
- Le panier nucléaire constitue une plateforme périphérique située immédiatement en aval de la traversée nucléaire.
- Il est positionné au contact de la chromatine périphérique, contribuant à l’organisation spatiale du noyau et au couplage topologique entre pore nucléaire et compartiment nucléoplasmique.
Interface avec la lamina nucléaire
Le complexe du pore nucléaire est mécaniquement intégré à la lamina nucléaire au niveau de sa face nucléoplasmique, concernant principalement l’anneau nucléaire et le panier nucléaire (Interactions of Chromatin with the Nuclear Lamina and Nuclear Pore Complexes 2023).
1. Certaines nucléoporines établissent des interfaces directes ou indirectes avec les lamines A/C.
- Nup153, localisée à la face nucléaire du pore et associée au panier nucléaire, peut interagir avec les lamines A/C et contribuer à l’ancrage du pore dans le réseau laminaire.
- TPR, composant majeur du panier nucléaire, est positionnée à proximité immédiate de la lamina et participe à l’organisation structurale de cette interface.
Remarque : Elys se lierait directement à la chromatine, contribuant à l’ancrage des loci au pore nucléaire.
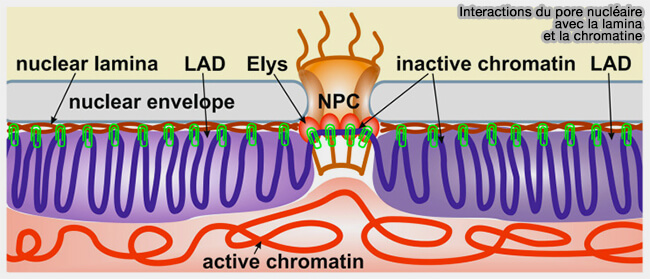
(Figure : vetopsy.fr d'après Shevelyov)
2. Ces interactions assurent une continuité mécanique entre l’anneau nucléaire du NPC, le réseau de lamines sous-jacent et la membrane nucléaire interne, contribuant à :
- la stabilité mécanique globale de l’enveloppe nucléaire,
- l’organisation de la chromatine périphérique,
- la coordination avec les systèmes mécaniques de l’enveloppe, notamment le complexe LINC.
Dynamique structurale du pore nucléaire
Le complexe du pore nucléaire n’est pas une structure rigide, mais un assemblage macromoléculaire dynamique capable d’adaptations conformationnelles et de réorganisations à deux niveaux (The Nuclear Pore Complex: Birth, Life, and Death of a Cellular Behemoth (2022) :
- une dynamique liée au cycle cellulaire,
- une dynamique locale et différentielle en interphase.
Dynamique au cours du cycle cellulaire
1. Lors de la rupture de l'enveloppe nucléaire en prométaphase, les pores nucléaires se désintègrent, non pas en protéines isolées, mais en modules structuraux conservés (Building a nuclear envelope at the end of mitosis: coordinating membrane reorganization, nuclear pore complex assembly, and chromatin de-condensation 2012).
- Les nucléoporines périphériques et les nucléoporines FG sont dissociées précocement.
- Les sous-complexes de la charpente protéique centrale, dont le complexe en Y, sont relocalisés dans le cytoplasme sous forme de sous-unités préservées.
- Les nucléoporines transmembranaires restent associées aux membranes issues de l'enveloppe nucléaire.
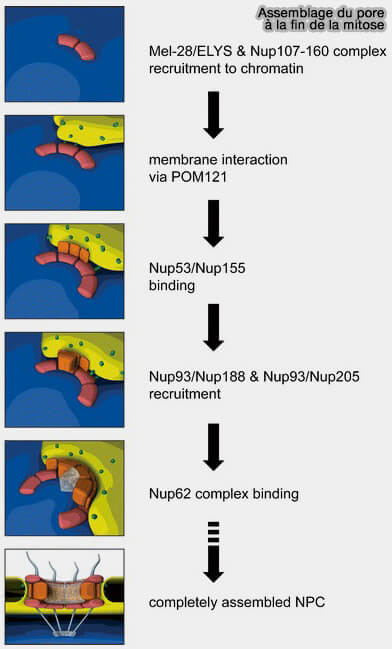
(Figure : vetopsy.fr d'après Schooley et coll)
2. Lors de la reformation de l’enveloppe nucléaire à la fin de l'anaphase et en télophase :
- les membranes nucléaire interne et externe se réassocient autour de la chromatine.
- les nucléoporines transmembranaires définissent des sites d’assemblage.
- les modules de la charpente protéique centrale sont recrutés séquentiellement.
- la barrière FG est réétablie secondairement.
Dynamique
en interphase
En interphase, le complexe du pore nucléaire conserve une architecture globalement stable tout en présentant une dynamique locale différenciée (Mechanisms of nuclear pore complex assembly – two different ways of building one molecular machine 2017).
1. De nouveaux pores peuvent être insérés dans l’enveloppe nucléaire intacte.
Ce processus implique :
- une déformation locale coordonnée des membranes interne et externe,
- le recrutement progressif des nucléoporines due la charpente centrale,
- la mise en place secondaire des nucléoporines FG.
2. Les sous-modules du NPC ne présentent pas la même dynamique, ce qui permet au pore de maintenir une architecture stable tout en conservant une capacité d’adaptation aux contraintes mécaniques et aux exigences du transport nucléocytoplasmique (Nuclear pore complex – a coat specifically tailored for the nuclear envelope 2012).
- Les éléments des anneaux sont globalement stables.
- Certaines nucléoporines périphériques ou riches en répétitions FG présentent un renouvellement plus rapide, reflétant la plasticité fonctionnelle du complexe.
3. La géométrie du canal central peut varier en fonction de l’état fonctionnel du pore, la symétrie radiale globale du complexe demeure conservée.
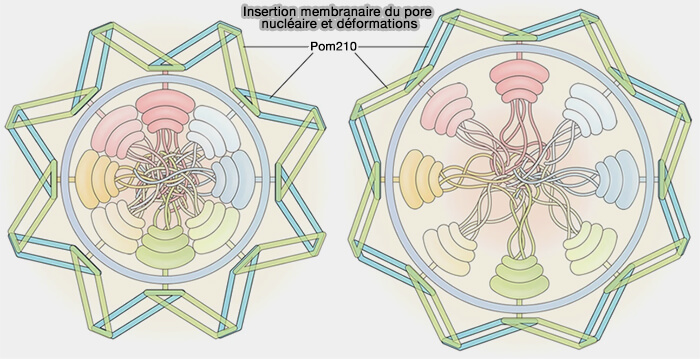
(Figure : vetopsy.fr d'après Yang et coll)
a. Ces variations sont observées :
- lors du passage de cargos de grande taille, qui déplacent transitoirement les chaînes FG,
- lors d’une forte activité de transport entraînant une occupation accrue du canal par des récepteurs liés aux motifs FG.
b. Ces situations entraînent :
- une dilatation ou un resserrement relatif du canal interne,
- une redistribution de la matrice FG dans la lumière du canal,
- une modification transitoire de l’occupation volumique centrale.
Transport nucléocytoplasmique
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauEnveloppe nucléairePores nucléairesLaminaCorps nucléairesTransport nucléocytoplasmiqueCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesMicrotubulesReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


