Noyau
Pores nucléaires
Transport nucléocytoplasmique : export
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

L’export nucléocytoplasmique repose sur la reconnaissance des signaux NES par les exportines couplées à Ran-GTP, assurant le transfert vectoriel des macromolécules du noyau vers le cytoplasme.
L’export nucléaire constitue le volet sortant du transport nucléocytoplasmique et assure le transfert directionnel des protéines et complexes macromoléculaires du compartiment nucléaire vers le cytoplasme.
Ce processus débute par la reconnaissance de signaux d’export nucléaire (NES) portés par les cargos, suivie de leur association avec des récepteurs de transport de la famille des karyophérines, appelés exportines, avant leur translocation à travers le complexe du pore nucléaire (NPC) sous le contrôle du gradient de Ran.
Signaux d’export nucléaire (NES)
L’export des protéines repose sur la présence de signaux d’export nucléaire (NES), séquences peptidiques spécifiques reconnues par les exportines.
1. Les NES leucine-rich sont généralement riches en résidus hydrophobes, en particulier leucine, isoleucine, valine, phénylalanine ou méthionine.
- Ils suivent un motif dégénéré caractérisé par l’espacement régulier de résidus hydrophobes, souvent représenté sous la forme Φ-X2,3–Φ–X2,3–Φ–X–Φ où Φ représente un résidu hydrophobe et X tout autre acide aminé.
- Ces séquences adoptent fréquemment une conformation hélicoïdale ou étendue permettant l’exposition spatiale des résidus hydrophobes nécessaires à la reconnaissance par l’exportine.
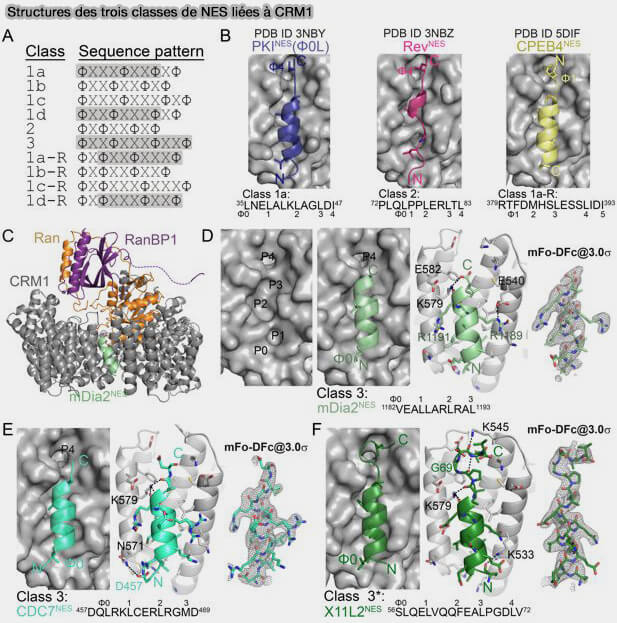
(Figure : vetopsy.fr d'après Fung et coll)
2. Sur le plan structural, ces résidus hydrophobes s’insèrent dans des poches hydrophobes successives (Φ0–Φ4) formées par le sillon longitudinal de l'exportine CRM1, définissant plusieurs classes géométriques selon leur mode d’occupation (Nuclear export receptor CRM1 recognizes diverse conformations in nuclear export signals 2017).
- La classe 1 correspond à une occupation séquentielle des poches hydrophobes dans une orientation canonique, comme celle de PKIα, petite protéine régulatrice endogène de la protéine kinase A (PKA), dont le NES LALKLAGLD est le plus étudié.
- La classe 2 présente une orientation inversée du peptide dans la gorge hydrophobe, comme celle de HIV-1 Rev.
- La classe 3 regroupe des NES présentant un espacement distinct des résidus hydrophobes tout en conservant l’engagement des poches Φ, comme Snurportin-1.
Remarque : une classification plus large incluant des NES atypiques ou contextuels a été proposée dans des travaux de synthèse récents (The nuclear export receptor CRM1/XPO1 and its diverse cargoes 2025).
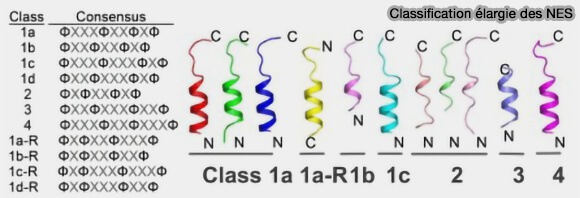
(Figure : vetopsy.fr d'après Kehlenbach et Chook)
3. Contrairement à l’import, la reconnaissance du NES par l’exportine est fortement dépendante de la présence de Ran-GTP (
- Dans le noyau, l’exportine adopte une conformation compatible avec la fixation du NES uniquement lorsqu’elle est associée à Ran-GTP pour former un complexe trimérique cargo–exportine–Ran-GTP.
- Cette dépendance garantit que l’assemblage du complexe d’export ne se produit que dans l’environnement nucléaire riche en Ran-GTP.
4. L’exposition d’un NES peut être contrôlée par :
- la phosphorylation, par exemple celle de FOXO par Akt, qui favorise son interaction avec les protéines 14-3-3 et stabilise une conformation exposant un NES fonctionnel reconnu par CRM1, entraînant son export cytoplasmique,
- des interactions intramoléculaires, comme pour Plk1, dont le NES peut être masqué ou exposé selon l’état d’activation et les interactions entre le domaine kinase et le domaine Polo-box ;
- la formation de complexes multiprotéiques, par exemple MDM2, qui contient un NES fonctionnel et peut favoriser l’export de p53 en recrutant CRM1.
Exportines
Les exportines appartiennent à la famille structurale des karyophérines β-like.
Elles partagent la même architecture en répétitions HEAT formant une superhélice flexible, mais sont spécialisées dans le transport nucléocytoplasmique du noyau vers le cytoplasme.
Contrairement aux importines, les exportines reconnaissent leurs cargos uniquement en présence de Ran lié au GTP.

Vous pouvez lire : The nuclear export receptor CRM1/XPO1 and its diverse cargoes (2025).
CRM1/XPO1 : exportine majeure
1. CRM1 (Chromosome Region Maintenance 1), également appelée XPO1, est l’exportine la plus largement étudiée et la principale responsable de l’export des protéines porteuses d’un NES leucine-rich.
a. CRM1 est composée de 21 répétitions HEAT (H1-H21), d'environ 40–50 résidus, chacune formée de deux hélices antiparallèles A (face convexe externe) et B (face concave interne).
L’ensemble forme un anneau flexible, capable d’adopter des conformations ouvertes ou fermées selon l’état de liaison à Ran-GTP et au cargo.
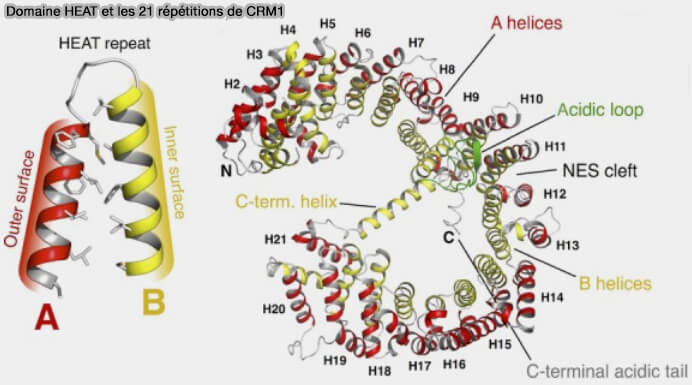
(Figure : vetopsy.fr d'après Striegl et coll)
b. La région N-terminale (H1–H3) est l'interface majeure de liaison à Ran-GTP qui stabilise la conformation fermée de CRM1 lors de la formation du complexe d’export.
c. La région médiane (H8–H12) constitue le cœur structural du sillon hydrophobe de liaison des NES.
- Les hélices A de H11 et H12 forment la gorge principale où s’insèrent les résidus hydrophobes Φ du NES.
- H9 joue un rôle de relais allostérique entre le site Ran et la gorge NES.
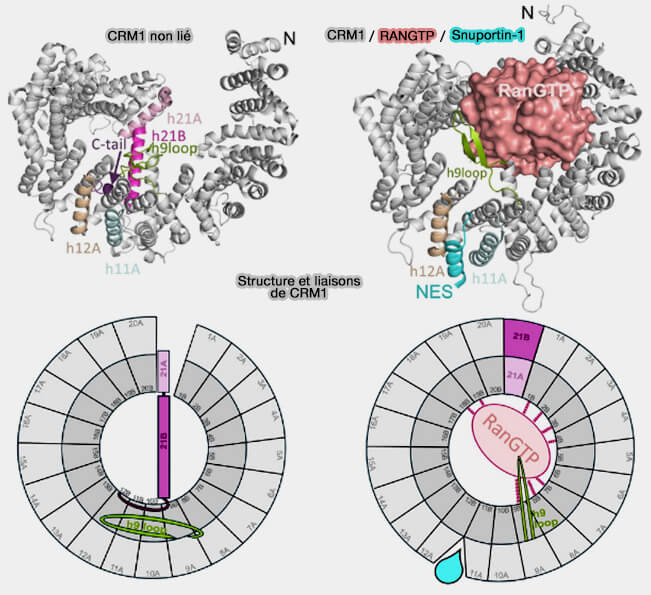
(Figure : vetopsy.fr d'après Kehlenbach et Chook)
d. La répétition H21 constitue l’élément terminal du solénoïde HEAT et adopte une organisation atypique par rapport aux répétitions précédentes et est prolongée par l'hélice C-terminale supplémentaire (C-helix).
- En l'absence de Ran-GTP, H21 adopte une conformation qui traverse le plan de l’anneau HEAT, tandis que l'hélice C-terminale interagit avec les hélices B des répétitions médianes (notamment H8–H12), contribuant à une conformation moins favorable à la fixation du NES.
- La liaison de Ran-GTP induit un réarrangement global du solénoïde, repositionnant la région C-terminale et stabilisant la conformation compétente pour l’engagement du NES, permettant la formation du complexe trimérique cargo–CRM1–Ran-GTP.

Cette dépendance structurale à Ran-GTP distingue les exportines des importines, dont la reconnaissance du cargo ne requiert pas la présence de Ran.
Autres exportines
Bien que CRM1 soit l’exportine la plus étudiée, il existe d’autres exportines spécialisées, appartenant également à la famille des karyophérines β-like et partageant une dépendance au Ran-GTP pour l’assemblage nucléaire des complexes d’export.
- CAS est responsable de l’export de l’importine α.
- L'exportine-t participe à l’export des ARN de transfert.
- L'exportine-5 est impliquée dans l’export des pré-miARN.
- L'exportine-4 contribue au transport nucléaire de certaines protéines régulatrices.
Remarque : l’export des ARN (ARNm, ARNt, pré-miARN) repose sur des exportines spécialisées ou sur des adaptateurs protéiques associés aux complexes ribonucléoprotéiques.
Ces cargos volumineux utilisent le même principe de dépendance au Ran-GTP, mais impliquent des interfaces supplémentaires et des mécanismes de surveillance nucléaire.
Mécanisme de l'export nucléaire
Assemblage nucléaire du complexe d’import
Dans le noyau, la concentration élevée en Ran-GTP favorise la formation d’un complexe ternaire stable associant :
- le cargo porteur d’un NES,
- l’exportine (principalement CRM1/XPO1),
- Ran-GTP.
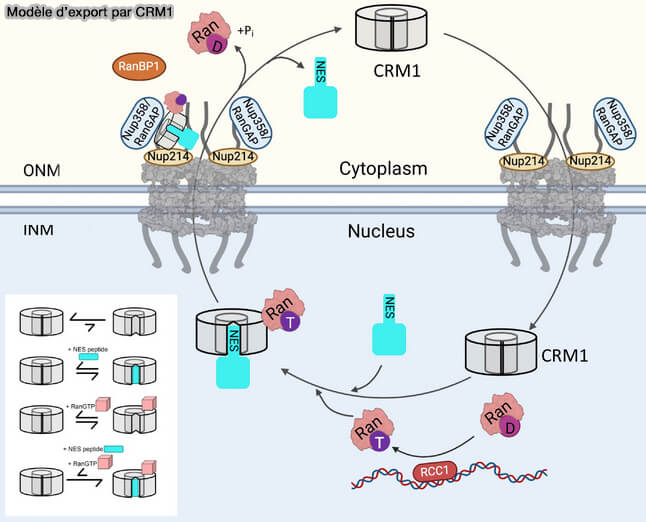
(Figure : vetopsy.fr d'après Kehlenbach et Chook)
1. La liaison de Ran-GTP stabilise une conformation de CRM1 compétente pour la reconnaissance du NES, conditionnant l’assemblage du complexe d’export (
2. La reconnaissance du NES repose sur l’insertion stéréospécifique de résidus hydrophobes du cargo dans des poches alignées le long du sillon formé par les répétitions H11 et H12 de CRM1.
- La liaison du NES et celle de Ran-GTP sont coopératives, Ran-GTP stabilise la géométrie du sillon, tandis que l’engagement du NES rigidifie l’interface Ran–CRM1.
- Le complexe trimérique cargo–CRM1–Ran-GTP ne devient stable que dans l’environnement nucléaire enrichi en Ran-GTP.
Translocation du complexe d’export à travers le pore nucléaire
Le complexe cargo–CRM1–Ran-GTP, préalablement assemblé dans le noyau, diffuse jusqu’à l’interface nucléaire du pore et interagit avec les nucléoporines riches en répétitions FG.
1. La progression à travers le canal central repose sur des interactions multivalentes et transitoires entre :
- les surfaces hydrophobes de CRM1,
- les résidus phénylalanine des répétitions FG.
Le complexe d’export est déjà thermodynamiquement stabilisé avant son entrée dans le pore et le NPC ne sélectionne pas le cargo, mais assure la progression d’un complexe compétent.
2. La translocation s’effectue par diffusion facilitée au sein du réseau dense de nucléoporines FG, selon une succession rapide d’associations et dissociations analogues à celles décrites pour les importines (
- Aucun moteur mécanique ni hydrolyse d’ATP n’intervient au niveau du pore.
- La directionnalité du transport ne résulte pas d’une asymétrie structurale du pore nucléaire, mais du gradient nucléocytoplasmique de Ran, caractérisé par une forte concentration de Ran-GTP dans le noyau et de Ran-GDP dans le cytoplasme.
Dissociation cytoplasmique
1. Une fois exposé du côté cytoplasmique du pore, le complexe cargo–CRM1–Ran-GTP entre en contact avec des protéines contenant des domaines Ran-binding (RBD) :
- RanBP1, protéine cytoplasmique soluble,
- Nup358 (RanBP2), localisée sur les filaments cytoplasmiques du pore.
a. Ces protéines se lient à Ran-GTP et stabilisent une conformation spécifique des régions Switch I et Switch II, induisant un réarrangement de l’interface Ran–CRM1.
b. L’engagement du domaine RBD provoque un repositionnement des régions Switch qui :
- réduit la surface de contact stabilisatrice entre Ran-GTP et CRM1,
- expose davantage Ran à l’action de RanGAP.
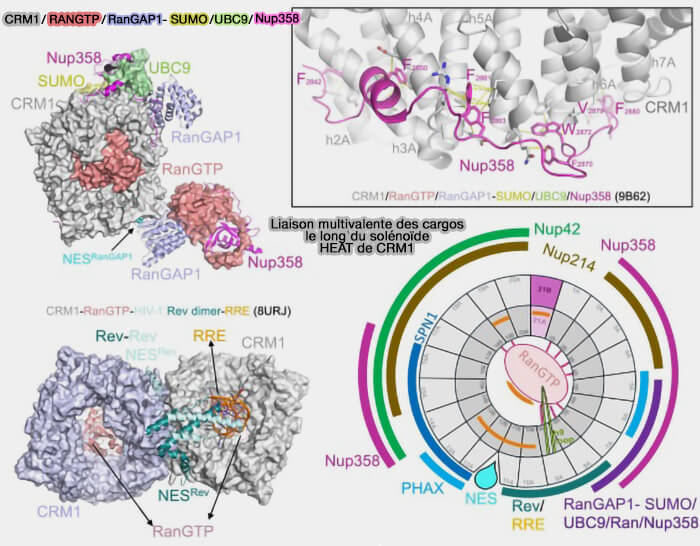
(Figure : vetopsy.fr d'après Kehlenbach et Chook)
2. RanGAP est ancrée du côté cytoplasmique du pore par son interaction avec Nup358, qui agit comme plateforme d’assemblage.
a. Nup358 est SUMOylée et recrute le complexe RanGAP–Ubc9, ce qui positionne RanGAP à proximité immédiate des complexes d’export sortants.
b. RanGAP catalyse l’hydrolyse du GTP lié à Ran, entraînant :
- une transition conformationnelle majeure des régions Switch I et II, la conversion Ran-GTP ➞ Ran-GDP,
- la perte de compatibilité structurale entre Ran et CRM1.
3. L’hydrolyse du GTP rompt la coopération thermodynamique qui stabilisait le complexe cargo–CRM1–Ran-GTP, ce qui provoque :
- la dissociation de Ran-GDP,
- la perte d’affinité de CRM1 pour le NES,
- la libération du cargo dans le cytoplasme.
Remarque : certains ARN ne possèdent pas de signal peptidique de type NES et leur export dépend d’adaptateurs protéiques (par exemple PHAX pour les snARN ou Rec/Rev pour certains ARN viraux) qui recrutent CRM1–Ran-GTP via un NES porté par la protéine adaptatrice.
Le principe mécanistique demeure identique, i.e. assemblage nucléaire trimérique dépendant de Ran-GTP, translocation via les nucléoporines FG et dissociation cytoplasmique après hydrolyse du GTP.
Recyclage des composants
1. CRM1, libérée sous forme libre dans le cytoplasme, retourne vers le noyau par diffusion facilitée à travers le pore nucléaire, grâce aux interactions transitoires entre ses répétitions HEAT et les nucléoporines riches en motifs FG.
Ce retour résulte de la dynamique bidirectionnelle intrinsèque des karyophérines et du gradient nucléocytoplasmique de Ran, qui maintient une faible concentration de CRM1 liée à Ran dans le cytoplasme et favorise son recyclage nucléaire.
2. Ran-GDP, incapable de diffuser efficacement seul à travers le pore, est pris en charge par le transporteur spécifique NTF2 (Nuclear Transport Factor 2) pour régagner le noyau, où l’échange GDP/GTP sera catalysé par RCC1 (
Remarque : une synthèse comparative présente côte à côte les étapes clés et les déterminants moléculaires de l’import et de l’export nucléaires, afin de mettre en évidence leur organisation symétrique ainsi que leurs divergences mécanistiques essentielles.
Retour aux pores nucléaires ou au noyau
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauEnveloppe nucléairePores nucléairesLaminaCorps nucléairesTransport nucléocytoplasmiqueCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesMicrotubulesReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


