Cytosquelette : filaments intermédiaires de type V
Lamines : rôles
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Les lamines nucléaires assurent des fonctions mécaniques, organisationnelles et régulatrices essentielles, reliant l’architecture du noyau à la dynamique cellulaire, à l’expression génique et aux pathologies associées.
Les lamines, filaments intermédiaires de classe V, interviennent à plusieurs niveaux complémentaires du fonctionnement cellulaire (The nuclear lamins: flexibility in function 2013).
Leur rôle ne se limite pas à une fonction de charpente du noyau, mais s’étend à des dimensions mécaniques, organisationnelles, fonctionnelles et pathologiques (The lamin protein family 2011) :
- le couplage mécanique entre le noyau et le cytosquelette, qui confère au noyau des propriétés mécaniques adaptées aux contraintes cellulaires,
- les rôles dans l’organisation de la chromatine et l’expression génique, mettant en évidence leur implication dans la régulation fonctionnelle du génome,
- la migration cellulaire et les cancers, où la déformabilité nucléaire devient un facteur limitant majeur,
- les laminopathies, illustrant les conséquences pathologiques des altérations des lamines sur les tissus et l’organisme.
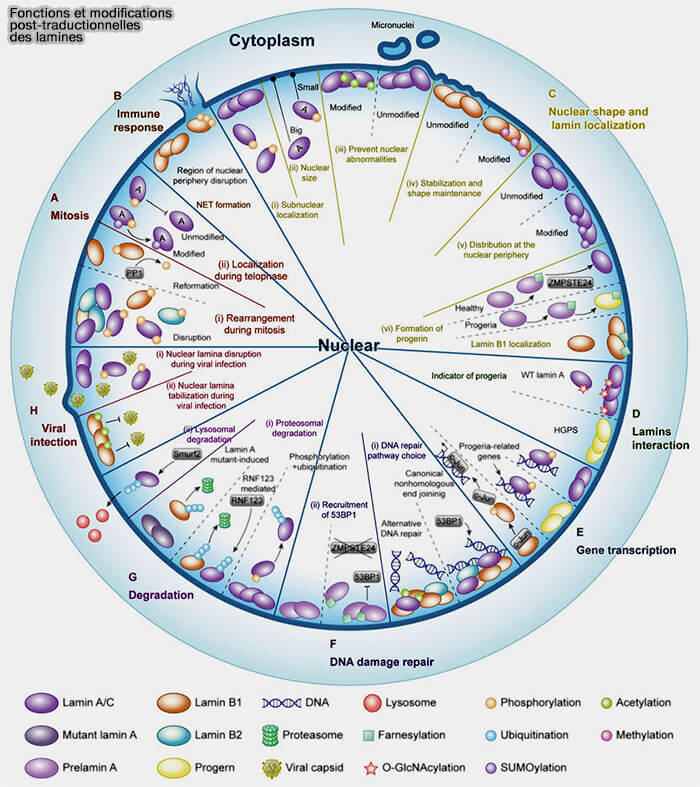
(figure : vetopsy.fr d'après Zheng et col)
Couplage mécanique entre le noyau et le cytosquelette
Les lamines nucléaires, en particulier les lamines A/C, jouent un rôle central dans le couplage mécanique entre le noyau et le cytosquelette cytoplasmique, i.e. filaments d'actine, microtubules cytoplasmiques et filaments intermédiaires.
1. En formant la lamina nucléaire sous-jacente à la membrane nucléaire interne, elles constituent une plateforme d’ancrage essentielle pour la transmission des forces mécaniques exercées sur le noyau.
Les lamines contribuent ainsi :
- à la résistance du noyau aux contraintes mécaniques,
- au maintien de son intégrité structurale,
- à la limitation des déformations excessives de l’enveloppe nucléaire, notamment lors de la migration cellulaire ou de situations de stress mécanique important.
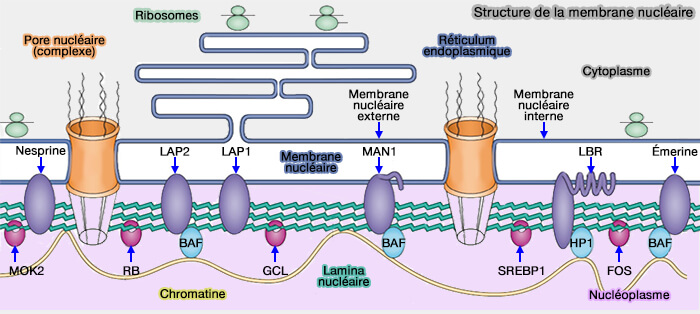
(Figure : vetopsy.fr d'après H. D. M Coutinho)
2. Ce couplage mécanique repose sur l’interaction des lamines avec des protéines transmembranaires de l’enveloppe nucléaire, en particulier les protéines SUN de la membrane nucléaire interne, qui assurent la continuité physique avec des complexes de la membrane nucléaire externe reliant le cytosquelette.

L’ensemble de cette continuité mécanique est assuré par le complexe LINC, formé par l'association des protéines SUN et KASH (nesprines) qui sont étudiées dans la page de l'enveloppe nucléaire.
3. Ainsi, les lamines nucléaires ne se limitent pas à un rôle structural passif, mais participent activement aux propriétés mécaniques globales de la cellule.
Remarque : la lamina nucléaire assure l’ancrage mécanique du complexe du pore nucléaire sur sa face nucléoplasmique, via des interactions établies principalement avec l’anneau nucléaire et les structures du panier nucléaire (
Rôles dans l’organisation de la chromatine et l’expression génique
1. Les lamines, en particulier les lamines A/C, participent à l’organisation spatiale du génome au sein du noyau et interagissent avec la chromatine (Lamins A and C but Not Lamin B1 Regulate Nuclear Mechanics 2006).
a. Elles contribuent au positionnement périphérique de domaines chromosomiques spécifiques, influençant ainsi :
- l’architecture nucléaire,
- la distribution des chromosomes,
- la compartimentation fonctionnelle entre euchromatine et hétérochromatine.
b. Par ces interactions, les lamines :
- jouent un rôle dans le maintien de l’intégrité de structures chromatiniennes particulières, notamment des télomères (Attenuated hypertrophic response to pressure overload in a lamin A/C haploinsufficiency mouse 2010),
- participent indirectement à la stabilité du génome (Attenuated hypertrophic response to pressure overload in a lamin A/C haploinsufficiency mouse 2010).
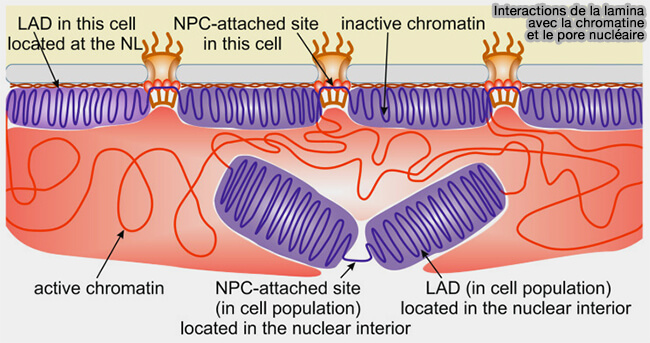
(Figure : vetopsy.fr d'après Shevelyov)
2. Les lamines influencent l’expression génique en modulant l’accessibilité de régions chromatiniennes et par la séquestration ou le relargage de facteurs de transcription.
Ces effets peuvent être médiés par des interactions directes avec les histones ou par l’intermédiaire de protéines associées à la chromatine, permettant aux lamines de participer à la régulation transcriptionnelle sans agir comme facteurs de transcription au sens strict.
3. Ces fonctions reposent sur un réseau d’interactions avec des protéines de la membrane nucléaire interne et du nucléosquelette.

Les protéines liées aux lamines sont étudiées dans un chapitre spécifique.
4. Ainsi, les lamines nucléaires occupent une position centrale à l’interface entre architecture nucléaire et régulation fonctionnelle du génome.
a. Par leur rôle dans la mécanotransduction nucléo-cytosquelettique et leurs interactions avec la chromatine, elles participent à :
- la modulation des voies de signalisation et de la transcription,
- la régulation de processus nucléaires fondamentaux tels que la réplication de l’ADN et la progression du cycle cellulaire, en lien étroit avec l’organisation chromatinienne.
b. Toute altération de ces interactions, qu’elle soit d’origine mécanique, génétique ou pathologique, peut se traduire par des modifications profondes des programmes transcriptionnels et des processus nucléaires associés, à l'origine des laminopathies.
Migration cellulaire (et cancers)
Lors de la migration cellulaire en environnement tridimensionnel, le noyau constitue une contrainte mécanique majeure.
Contrairement à la migration bidimensionnelle, la progression des cellules dans des matrices 3D implique le franchissement de confinements étroits, faisant de la capacité du noyau à se déformer un facteur limitant déterminant du processus migratoire (The distinct roles of the nucleus and nucleus-cytoskeleton connections in three-dimensional cell migration 2012).
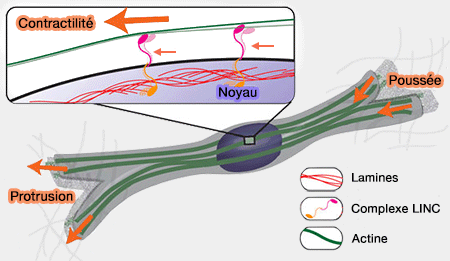
(Figure : vetopsy.fr d'après Khatau)
1. La composition de la lamina nucléaire, en particulier le niveau d’expression des lamines A/C, influence directement la déformabilité du noyau.
- Dans de nombreux contextes tumoraux, une diminution de la lamine A est associée à une augmentation de la plasticité nucléaire, permettant aux cellules de traverser plus efficacement des constrictions de taille micrométrique, favorisant ainsi l’invasion et la dissémination cellulaire (Nuclear Envelope Composition Determines the Ability of Neutrophil-type Cells to Passage through Micron-scale Constrictions 2013).
- À l’inverse, dans l'HGPS (syndrome de Hutchinson-Gilford), l’accumulation de progérine rigidifie la lamina et l’enveloppe nucléaire, réduisant fortement la capacité du noyau à se déformer et inhibant la migration cellulaire dans des environnements confinés.
2. Au-delà de ce rôle limitant, la déformabilité nucléaire influence en retour la dynamique du cytosquelette et le comportement migratoire global de la cellule (Squish and squeeze — the nucleus as a physical barrier during migration in confined environments 2016).
Le noyau agit ainsi comme une barrière physique interne dont les propriétés mécaniques conditionnent :
- l’organisation cytoplasmique,
- la persistance directionnelle,
- l’efficacité de la migration cellulaire dans des environnements contraints.
Laminopathies
Les lamines nucléaires, en particulier les lamines A/C, sont impliquées dans un ensemble de maladies génétiques rares regroupées sous le terme de laminopathies (When Lamins Go Bad: Nuclear Structure and Disease 2013).
1. Elles comprennent environ 450 maladies différentes, notamment :
- l'HGPS (Hutchinson-Gilford Progeria Syndrome ou Progeria), caractérisé par un vieillissement prématuré (Molecular ageing in progeroid syndromes: Hutchinson-Gilford progeria syndrome as a model 2009),
- l'EDMD (Emery–Dreifuss Muscular Dystrophy),
- la DCM (Dilated CardioMyopathy),
- la FPLD (Familial Partial Lipodystrophy Dunnigan-type).
La diversité des laminopathies illustre le rôle central des lamines A/C dans le maintien de l’architecture nucléaire, la mécanique cellulaire et la régulation fonctionnelle du noyau.

Des informations complémentaires sont disponibles dans : The UMD-LMNA mutations database.
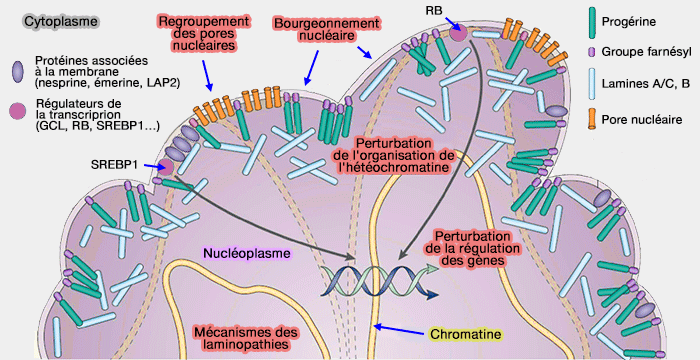
(Figure : vetopsy.fr d'après H. D. M Coutinho)
2. La plupart des cellules différenciées expriment au moins une lamine A.
a. Toutefois, certaines cellules présentent une expression faible ou absente de la lamine A comme :
- les cellules souches embryonnaires,
- les cellules de la couche inférieure de l'épiderme (Differential Expression of A-Type and B-Type Lamins during Hair Cycling 2009),
- les cellules du système nerveux central (Regulation of prelamin A but not lamin C by miR-9, a brain-specific microRNA 2012)
Cette distribution différentielle explique en partie la relative préservation du système nerveux central dans les laminopathies liées au gène LMNA.
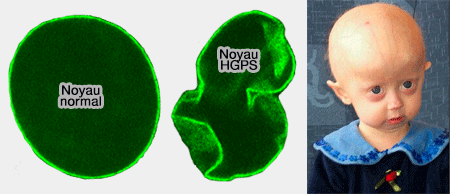
(Figure : vetopsy.fr d'après Scaffidi)
b. À l’inverse, les muscles striés, le tissu cardiaque et de nombreuses cellules mésenchymateuses expriment fortement les lamines A/C.
- Cela les rend particulièrement sensibles aux altérations de la structure ou de la dynamique de la lamina nucléaire.
- Une déficience en lamine A/C altère les propriétés mécaniques du noyau, le rendant plus déformable et plus fragile, et peut conduire à des anomalies de l’enveloppe nucléaire, voire à des ruptures transitoires de celle-ci sous contrainte mécanique.
3. Les lamines de type B jouent également un rôle essentiel dans l’intégrité nucléaire.
a. Leur déficience peut entraîner la formation de protrusions nucléaires (blebs) associées à une extrusion anormale de matériel génétique.
b. Les lamines B sont impliquées dans plusieurs processus cellulaires, notamment :
- dans l'organogenèse (Mouse B-Type Lamins Are Required for Proper Organogenesis But Not by Embryonic Stem Cells 2011), et en particulier dans le développement du système nerveux (A Mechanism for Nuclear Positioning in Fission Yeast Based on Microtubule Pushing 2011),
- dans la régulation de la prolifération et de la sénescence cellulaire par la lamine B1, ses variations d’expression ayant des effets opposés sur ces processus (Lamin B1 fluctuations have differential effects on cellular proliferation and senescence 2013).
Retour aux filaments intermédiaires
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesIFAPLaminesMicrotubulesMatrice extracellulaireReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


