Cytosquelette
Filaments intermédiaires (IF) : IFAP (Intermediate Filament Associated Protein)
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Les IFAP sont des protéines associées aux filaments intermédiaires qui assurent leur ancrage, leur organisation spatiale et leur intégration fonctionnelle avec les autres réseaux cellulaires.
Les protéines associées aux filaments intermédiaires (IFAP) constituent un ensemble hétérogène de facteurs qui ne participent pas directement à la polymérisation des filaments intermédiaires., mais qui en conditionnent l’organisation, l’ancrage et l’intégration fonctionnelle dans l’architecture cellulaire.
Elles assurent la connexion des filaments intermédiaires avec d’autres éléments du cytosquelette, les membranes cellulaires et certaines structures spécialisées, contribuant ainsi à la cohésion mécanique et à la stabilité des cellules.
Les IFAP sont abordées selon deux niveaux complémentaires :
- d’une part, la famille des plakines, qui constitue le groupe le plus structurant de protéines de liaison aux filaments intermédiaires,
- d’autre part, un ensemble d’IFAP spécialisées, exprimées de manière tissu-spécifique ou impliquées dans des fonctions particulières, telles que l’organisation musculaire, la différenciation épithéliale ou le couplage périnucléaire des filaments intermédiaires.
Plakines
Protéines de la famille des plakines
Les plakines constituent une famille de protéines de liaison reliant le cytosquelette aux structures membranaires et assurant l’intégration mécanique des filaments intermédiaires avec les autres réseaux cytosquelettiques.
1. Cette famille comprend actuellement sept membres (Plakins, a Versatile Family of Cytolinkers: Roles in Skin Integrity and in Human Diseases 2014) :
- la plectine,
- BPAG1/dystonine (Bullous Pemphigoid Antigen 1), impliquée dans l’ancrage des filaments intermédiaires aux microtubules et à l’actine, ainsi que dans l’organisation axonale et la stabilité neuronale,
- la desmoplakine, assurant l’ancrage des filaments intermédiaires aux desmosomes et contribuant à la cohésion mécanique des épithéliums,
- ACF7/MACF1 (Microtubule–Actin Cross-linking Factor 1), impliquée dans le couplage entre microtubules, actine et filaments intermédiaires, ainsi que dans la polarité et la migration cellulaire,
- l'envoplakine, participant à l’organisation de la couche cornée de l’épiderme et au renforcement mécanique des kératinocytes différenciés,
- la périplakine, établissant un lien entre les kératines et la membrane plasmique, contribuant à la stabilisation du cortex actinique cellulaire,
- l'épiplakine, dont l’association étendue aux réseaux de kératines renforce la résistance structurale des épithéliums soumis à des contraintes mécaniques.
2. Les spectraplakines constituent une sous-famille de plakines, caractérisée par la présence de répétitions de spectrine et de domaines supplémentaires permettant le couplage des filaments intermédiaires avec l’actine et les microtubules comme MACF1/ACF7, BPAG1/dystonine.
Plectine
La plectine, protéine géante ubiquitaire, exprimée dans la plupart des tissus, joue un rôle central dans l’organisation et l’ancrage du réseau de filaments intermédiaires (Plectin isoforms as organizers of intermediate filament cytoarchitecture 2011).
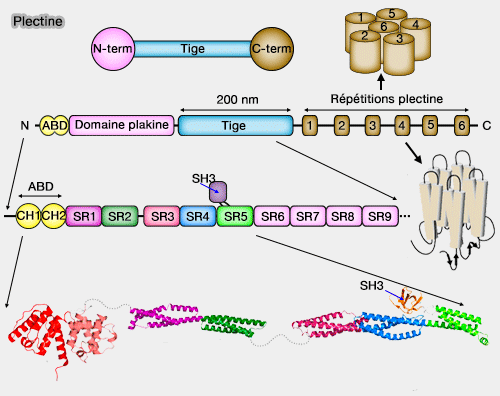
(Figure : vetopsy.fr)
Elle établit des liaisons multiples entre les filaments intermédiaires et :
- les autres réseaux cytosquelettiques, notamment les filaments d'actine ou les microtubules,
- la lamina nucléaire,
- les adhérences focales et les jonctions cellulaires en particulier, les desmosomes et les hémidesmosomes,
- la membrane plasmique.
Dans les muscles striés, la plectine interagit avec la desmine pour former des liaisons latérales entre les lignes Z voisines et cette organisation contribue à la cohésion mécanique du réseau myofibrillaire et favorise l’association étroite entre les myofibrilles et les mitochondries.
2. Par ces fonctions d’ancrage et de couplage cytosquelettique, la plectine contribue à la stabilité mécanique cellulaire et à la capacité de remodelage du cytosquelette lors de la migration.
Structure de la plectine
La structure de la plectine comporte les trois domaines classiques des IFAP.
1. Le domaine N-terminal comprend :
- un domaine ABD (Actin-Binding Domain), formé de deux domaines CH (Calponin Homology), qui se lie à l'intégrine α6β4, à la nesprine-3, à l'actine-F, à la dystrophine ou à la vimentine, et indirectement aux filaments intermédiaires via ces partenaires.
- un site de liaison à PIP2 (phosphatidylinositol-4,5-bisphosphate), localisé dans la région N-terminale de la plectine, qui régule son interaction avec l’actine et la nesprine-3.
Ce site, de nature basique et partiellement désordonnée, n’est pas résolu dans les structures tridimensionnelles disponibles.
- un domaine plakine (1070 résidus environ) impliqué dans la liaison aux filaments intermédiaires, formé de neuf répétitions de la spectrine (SR1 à SR9)
Chacune est constituée d’environ 100 résidus organisés en trois 3 hélices α amphipathiques, A, B et C, connectées par des boucles.
- un domaine SH3 (Src-Homology 3) enchâssé dans SR5 (The Structure of the Plakin Domain of Plectin Reveals an Extended Rod-like Shape 2016).
Le domaine SH3 interagit avec d'autres protéines telles que l'intégrine α6β4, le collagène de type XVII (appelé aussi BP180 ou BPAG2), le β-dystroglycane, la synémine et la kinase Fer.
2. La tige (rod domain) centrale (1250 résidus environ) permet la dimérisation de la plectine par formation de domaines coiled-coil (superhélice), donnant des homodimères parallèles et des oligomères d'ordre supérieur par association latérale, idéalement adaptés pour relier des protéines sur des distances relativement longues.
(Figure : vetopsy.fr)
3. Le domaine C-terminal contient six domaines PRD (Plectine Repeat Domain ou PLEC domain M1 à M6), d’environ 300 résidus chacun, structurellement apparentés aux répétitions ankyrine (ankyrin-like repeat domains) et organisés en solénoïde (Plectin repeats and modules: strategic cysteines and their presumed impact on cytolinker functions 2001).
a. Chaque PRD possède une région centrale comprenant des copies conservées du module plectine, motif de 38 résidus (2 x 19) répété 5 fois en tandem et reliés les uns aux autres par des segments variables.
Les domaines PRD forment une structure tertiaire globulaire stabilisée par des ponts disulfure et participent à la liaison de la plectine à l’intégrine β4 et au β-dystroglycane.
b. Un site unique de phosphorylation sur PRD6 est ciblé par le complexe cycline B/CDK1 (MPF) au cours de la mitose (M-Phase-specific Phosphorylation and Structural Rearrangement of the Cytoplasmic Cross-linking Protein Plectin Involve p34cdc2 Kinase 1996).
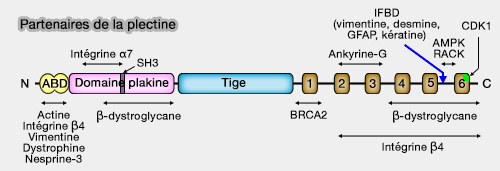
Partenaires de la plectine
La plectine interagit avec un grand nombre de partenaires, ce qui reflète son rôle central de cytolinker intégrant les filaments intermédiaires aux autres réseaux cytosquelettiques et aux structures cellulaires.
1. Le site principal de liaison aux filaments intermédiaires est localisé dans une région d’environ 50 résidus située entre les domaines PRD5 et PRD6.
a. Cette région interagit avec plusieurs types de filaments intermédiaires, notamment :
- la vimentine,
- la desmine,
- la GFAP,
- les cytokératines.
b. Ce site interagit également avec des partenaires de signalisation associés aux filaments intermédiaires, suggérant un lien entre organisation cytosquelettique et régulation métabolique, tels que :
- RACK1 (Receptor for Activated C Kinase 1), (RACK1, A multifaceted scaffolding protein: Structure and function 2011),
- la sous-unité γ1 de l'AMPK (AMP-activated protein kinase).
2. La plectine interagit avec la lamine B et avec la nesprine-3, contribuant au couplage mécanique entre le réseau de filaments intermédiaires cytoplasmiques et l’enveloppe nucléaire.
Ce lien participe à la transmission des forces mécaniques entre le cytoplasme et le noyau.
3. La plectine se lie indirectement au réseau microtubulaire par l’intermédiaire de protéines associées aux microtubules telles que MAP1 et MAP2 (Microtubule-Associated Proteins), ainsi qu’aux neurofilaments (sous-unités 210, 160 et 70 kDa), en particulier dans les cellules neuronales.
4. La plectine interagit avec des protéines des jonctions cellulaires, notamment la desmoplakine, participant ainsi à l’ancrage des filaments intermédiaires aux desmosomes et au renforcement de la cohésion mécanique des tissus épithéliaux (Plectin: A Cytolinker by Design 1999 et Role of plectin in cytoskeleton organization and dynamic 1998).
5. La plectine interagit avec BRCA2 (BReast Cancer 2) pour former un complexe cytosquelettique reliant indirectement le centrosome au réseau de filaments intermédiaires.
Cette interaction contribue à stabiliser la position du centrosome par rapport au reste de la cellule et participe au contrôle de la polarité cellulaire et de l’organisation spatiale du cytosquelette (BRCA2 interacts with the cytoskeletal linker protein plectin to form a complex controlling centrosome localization 2009).

Des mutations de la plectine provoquent des plectinopathies : myodystrophie, neuropathie, épidermolyse bulleuse (The many faces of plectin and plectinopathies: pathology and mechanisms 2013).
Autres IFAP
Outre les plakines, plusieurs protéines associées aux filaments intermédiaires assurent des fonctions spécialisées selon les tissus, contribuant à l’organisation mécanique, à l’ancrage périnucléaire ou à la différenciation cellulaire.
1. Certaines IFAP sont situées dans les muscles striés.
- La syncoiline est localisée au niveau de la ligne Z, où elle interagit avec la desmine et l'α-dystrobrévine et contribue à l’ancrage des filaments intermédiaires au complexe dystrophine-glycoprotéine et à la cohésion mécanique des myofibrilles.
- La paranémine, décrite notamment chez le poulet, est une protéine associée aux filaments intermédiaires musculaires impliquée dans l’organisation du cytosquelette strié.
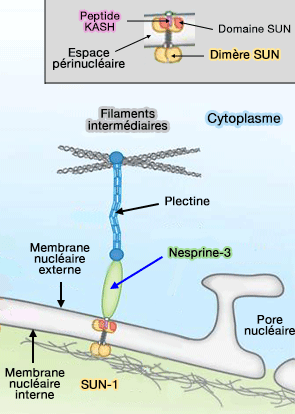
(Figure : vetopsy.fr
d'après Starr avec sa permission)
2. La filaggrine (FILament AGGRegating proteIN) s’associe aux filaments intermédiaires de kératines dans les kératinocytes différenciés, où elle favorise leur agrégation, contribuant à la formation de la couche cornée et à la fonction de barrière protectrice de l’épiderme.
3. La nesprine-3, une protéine KASH, est la seule nesprine à se lier indirectement aux filaments intermédiaires, via son interaction avec la plectine (Nesprin-3: a versatile connector between the nucleus and the cytoskeleton 2011 et Nesprin interchain associations control nuclear size 2012).
a. La nesprine-3, localisée dans la membrane nucléaire externe, participe au couplage mécanique entre le réseau de filaments intermédiaires et l’enveloppe nucléaire grâce à la plectine.
- En effet, les filaments intermédiaires ne sont pas directement ancrés à l’enveloppe nucléaire.
- Leur connexion au noyau repose sur des protéines adaptatrices qui assurent un lien mécanique entre le cytosquelette et l’enveloppe nucléaire.
Il existe cependant d’autres voies de couplage entre le noyau et le cytosquelette.
- Les nesprines 1 et 2 se lient directement aux filaments d’actine et assurent un couplage actine–noyau au sein du complexe LINC.
- Ces protéines représentent donc une voie distincte de connexion mécanique, indépendante des filaments intermédiaires.
b. Elle peut se lier aux microtubules par l'intermédiaire de BPAG1/dystonine (Bullous Pemphigoid Antigen 1) et MACF (Microtubule–Actin Cross-linking Factor), ces protéines assurant à leur tour des connexions avec le réseau d'actine et permettant l’intégration de l’ensemble du cytosquelette,
Retour aux filaments intermédiaires
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesIFAPLaminesMicrotubulesMatrice extracellulaireReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


