Cycle cellulaire
Interphase : préparation à la division cellulaire
Phase G1 :
croissance et préparation
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

L’interphase est la phase préparatoire du cycle cellulaire au cours de laquelle la cellule croît, réplique son ADN et prépare tous les éléments nécessaires à la division, assurant ainsi la continuité et l’intégrité du matériel génétique.
Le cycle cellulaire comprend plusieurs phases qui sont sous la dépendance des complexes cyclines/CDK.
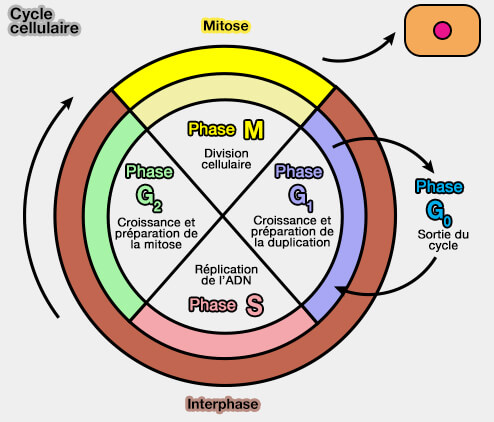
(Figure : vetopsy.fr d'après Zephris)
L’interphase correspond à l’ensemble des étapes du cycle cellulaire qui précèdent la division proprement dite et au cours desquelles la cellule assure sa croissance, la duplication de son génome et la mise en place des conditions nécessaires à la mitose, qui est classiquement subdivisée en trois phases successives.
- La phase G1 (de l'anglais growth, croissance ou gap, intervalle ou espace) est la première phase de croissance cellulaire (2n, 2c).
- La phase S (de l'anglais synthesis, synthèse) correspond à la réplication complète du matériel génétique (2n, 4c).
- La phase G2 est la dernière étape de l’interphase, qui a pour fonction principale de préparer la cellule à la mitose en vérifiant la complétude et l’intégrité du génome, tout en assurant la mise en place des structures nécessaires à la division cellulaire (2n, 4c).
Remarque : dans la convention utilisée dans vetopsy.fr, n correspond au nombre de chromosomes et c à la quantité totale d’ADN dans la cellule.
Ainsi, une cellule diploïde possède 2n chromosomes et contient 2c d’ADN en G1, 4c après réplication, 2c après méiose I et 1c après méiose II.
Phase G1
Croissance et préparation
1. La phase G1 (de l'anglais, growth, croissance ou gap, intervalle ou espace), est la première phase de croissance cellulaire (2n, 2c).
C’est la phase la plus longue du cycle, marquée par une synthèse cytoplasmique active de protéines et d’organites, qui entraîne une augmentation progressive de la taille cellulaire.

Cette croissance prépare la cellule à la réplication de l’ADN, en fournissant les ressources métaboliques et structurales nécessaires à l’entrée ultérieure en phase S.
2. Durant cette phase, un événement central est l’établissement de la compétence réplicative des origines, par l’assemblage des licensing factors conduisant à la formation du complexe de pré-réplicatif (pré-RC).
a. La chromatine est majoritairement sous forme d'euchromatine, configuration qui favorise l’accès aux facteurs nécessaires à la transcription et au licensing des origines.
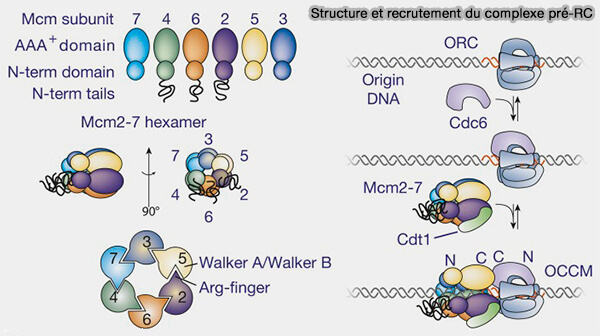
(Figure : vetopsy.fr d'après Bell et Labib)
b. Les origines de réplication sont rendues compétentes par l’assemblage des licensing factors pour former le complexe pré‑réplicatif (pré-RC), constitué par (Chromosome Duplication in Saccharomyces cerevisiae 2016) :
- les protéines ORC (Origin Recognition Complex ), i.e. ORC1-6, qui se fixent en premier sur l’origine de réplication et recrutent les autres facteurs,
- Cdc6 (cell division cycle 6), qui stabilise l’association d’ORC avec l’ADN et participe au chargement de l’hélicase,
- Cdt1 (Chromatin licensing and DNA replication factor 1), qui agit comme facteur de chargement du complexe MCM,
- le complexe MCM (MiniChromosome Maintenance protein complex), i.e. MCM2-7, hélicase réplicative chargée sur l’ADN sous forme inactive.
Cet assemblage définit un état d’origine " licenciée ", mais encore incapable d’initier la réplication.
Remarques sémantiques : une origine de réplication est un site défini du génome sur lequel s’assemblent les protéines nécessaires pour initier l’ouverture de l’ADN et le démarrage de la réplication.
Le terme licensing, littéralement " mise en capacité ", désigne le processus par lequel une origine de réplication est rendue compétente pour initier la réplication lors de la phase S suivante.
3. En fin de G1, la libération d’E2F consécutive à la phosphorylation de Rb par les complexes cycline D/CDK4-6 induit la transcription de la cycline E (
L’assemblage des complexes cycline E/CDK2 constitue l’événement terminal du passage du point de restriction (R) et prépare immédiatement l’activation des origines de réplication en début de phase S.
Point de restriction (R) et signaux mitogènes
1. À la fin de la phase G1, le point de restriction, appelé point R, constitue une étape décisionnelle majeure, intégrant des signaux internes et externes, qui détermine si la cellule :
- s’engage dans la phase S du cycle cellulaire pour répliquer son ADN,
- entre dans la phase G0, dite de quiescence, état dans lequel se trouvent la plupart des cellules différenciées et qui peut durer plus ou moins longtemps.
2. Le point R correspond ainsi à une décision d’engagement prolifératif dépendante du contexte mitogène, distincte des checkpoints de surveillance du génome.
Il coïncide fonctionnellement avec le principal seuil de la transition G1/S.
3. Toutefois, cette transition reste soumise à un mécanisme de surveillance distinct, le checkpoint G1/S, qui peut bloquer l’entrée en phase S en cas de dommages à l’ADN via l’activation de p53 et de p21.
Signaux externes
Les signaux externes sont des facteurs de croissance (growth factors), i.e. PDGF, FGF, and EGF, qui se fixent à leurs récepteurs à activité tyrosine kinase (RTK) à la surface cellulaire et déclenchent des cascades de phosphorylation intracellulaires.
1. La voie MAPK/ERK (Ras-Raf-MEK-ERK) finit par phosphoryler ERK qui se transloque ensuite dans le noyau où il active :
- l'expression de gènes précoce comme Fos et Myc,
- les dimères Fos/Jun qui forment le complexe de facteur de transcription AP-1 provoquent la transcription du gène CCND (cyclines D1, D2 ou D3).
Ces gènes induisent la synthèse de la cycline D1, essentielle à l’activation des complexes cycline D/CDK4-6.

La voie MAPK/ERK, étudiée dans un chapitre spécifique, constitue ainsi un lien fonctionnel direct entre signaux mitogènes et progression du cycle cellulaire.
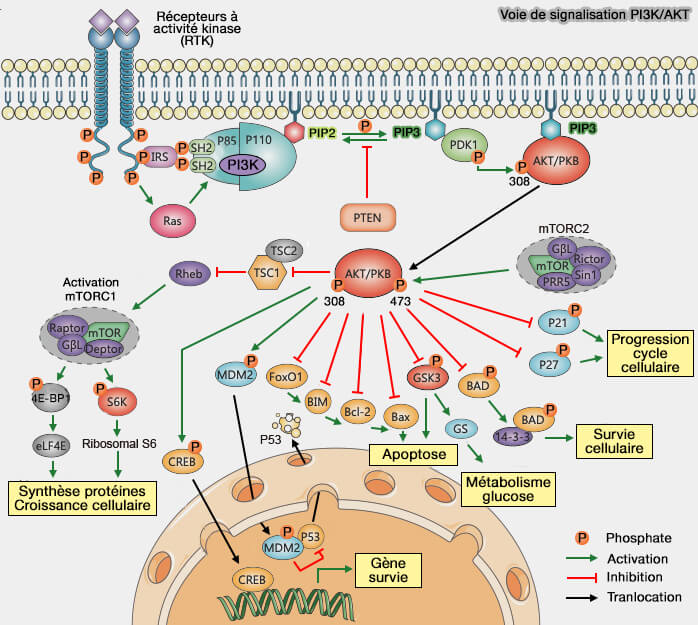
(Figure : vetopsy.fr d'après creative-diagnostic.com)
2. La voie PI3K/Akt est activée par p85, la sous-unité régulatrice de PI3K (Phosphatidylinositol 3-kinase de classe I), protéine contenant un domaine SH2 qui se lie aux RTK activés et stimule la traduction des ARNm des cyclines D et favorise la croissance cellulaire.
a. Cette interaction stimule la production de PIP3 à partir de PIP2, l’activation d’AKT, et conduit à la traduction des ARNm des cyclines D, favorisant ainsi la croissance et la progression en phase G1.

La voie PI3K/Akt, étudiée dans un chapitre spécifique, préserve la viabilité cellulaire et le métabolisme énergétique.
b. En outre, Akt régule les composants G1/S par :
- la promotion de la traduction de la cycline D1 par mTORC1, car l’ARNm de la cycline D1 fait partie des transcrits sensibles à la disponibilité d’eIF4E (
AKT et mTORC1),
- la phosphorylation des inhibiteurs de CDK, p27KIP1, pour prévenir son importation nucléaire, et de p21CIP1, pour diminuer sa stabilité,
- l'inactivation de la phosphorylation du facteur de transcription FOXO4, qui régule l'expression de p27.
Remarque : en G1 précoce, p21 et p27 agissent majoritairement comme cofacteurs d’assemblage des complexes cycline D/CDK4-6, en stabilisant le complexe, en favorisant sa localisation nucléaire et en permettant une activité basale suffisante pour engager la phosphorylation progressive de Rb.
3. Les signaux externes peuvent également être modulés par des voies contextuelles selon le type cellulaire, comme :
- la voie Wnt/β-caténine, qui peut activer directement la transcription de CCND1 dans de nombreux tissus (épithélium intestinal, foie, tumeurs colorectales),
- des mécanismes de crosstalk avec NF-κB et les signaux cytokiniques, particulièrement dans les cellules hématopoïétiques.
4. Ces signaux permettent la synthèse des cyclines D et l’activation des CDK4/6, en déstabilisant les CKI (CDK inhibitors).
Lors de leur absence, la cellule peut entrer en quiescence plutôt que de poursuivre le cycle.
Signaux internes
1. Les signaux internes dépendent de :
a. l'état métabolique, comme la disponibilité en ATP et en nucléotides pour la réplication de l’ADN, par l'activité de MTOR,
b. l'intégrité de l’ADN par la détection de dommages par :
- p53 qui peuvent arrêter le cycle en activant p21CIP1, un CKI (CDK inhibitors).
- ATM/ATR.
c. la taille et la croissance de la cellule car certaines cellules ne peuvent franchir le point R que si elles ont atteint un seuil de masse critique.
Ce seuil, variable selon le type cellulaire, est régulé par les voies métaboliques et de signalisation, notamment la voie PI3K/Akt, qui contrôlent la synthèse protéique et la croissance globale avant l’entrée irréversible en phase S.
2. L’expression des cyclines D dépend étroitement du microenvironnement cellulaire et des signaux d’adhésion.
a. Les intégrines, récepteurs transmembranaires liant la cellule à la matrice extracellulaire (MEC) activent la voie FAK (Focal Adhesion Kinase) et la voie Src, qui convergent vers MAPK et PI3K/AKT et maintiennent la transcription et la stabilité de la cycline D.
b. Lorsque la cellule perd son ancrage comme lors d’un détachement de la matrice ou atteint une densité de confluence élevée, ces voies d’adhésion sont inactivées par la diminution de la phosphorylation de FAK.
- Les signaux de survie et de croissance via AKT et ERK s’interrompent.
- La dégradation de la cycline D s’accélère par le protéasome, bloquant la progression du cycle.
Remarque : la notion de densité de confluence élevée désigne un état de surpopulation cellulaire dans un tissu ou une culture, où les cellules se touchent étroitement les unes les autres, occupant toute la surface disponible.
- Lorsqu’une cellule atteint une densité de confluence élevée, les contacts cellule-cellule, via les cadhérines activent des voies inhibitrices comme Hippo/YAP-TAZ ou p27KIP1, qui répriment la transcription des cyclines D et freinent les CDK4/6.
- Ce phénomène, appelé inhibition de contact, empêche les cellules normales de continuer à se diviser lorsque le tissu est complet.

Ce processus empêche les cellules normales de proliférer sans contact adéquat avec la matrice, limitant ainsi la prolifération anarchique observée dans les cellules tumorales où cette régulation est souvent abolie.
Rôles des cyclines/CDK
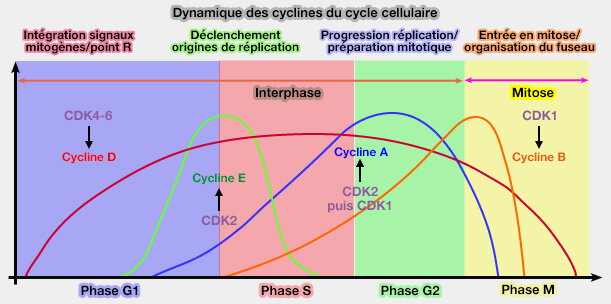
(Figure : vetopsy.fr)
1. En fin de mitose, l’activité du complexe APC/CCdh1, élimine massivement les cyclines A et B, réinitialisant l’appareil cycline/CDK et garantissant l’inactivation complète de CDK1.
a. Cette activité élevée persiste en début de G1, où elle contribue à :
- éliminer les cyclines A et B résiduelles,
- maintenir CDK1 totalement inactif, i.e. l'absence des cyclines A et B inhibe toute formation de complexes cycline/CDK1,
- - stabiliser un environnement cellulaire compatible avec une progression ordonnée vers la phase S.
(Figure : vetopsy.fr d'après Topacio et coll)
b. Cette " remise à zéro " du système cycline/CDK après la mitose maintient une G1 initiale strictement dépourvue de signaux mitotiques résiduels.
Remarque : CDK2 demeure bas tant que la cycline E n’est pas induite par E2F, empêchant la constitution prématurée de complexes cycline E/CDK2 et garantissant que l’entrée en phase S ne soit déclenchée qu’au moment opportun.
2. Une fois que les signaux internes et externes sont jugés favorables, les cycline D sont synthétisées et s’associent aux CDK4-6, formant les premiers complexes cycline/CDK actifs du cycle cellulaire.
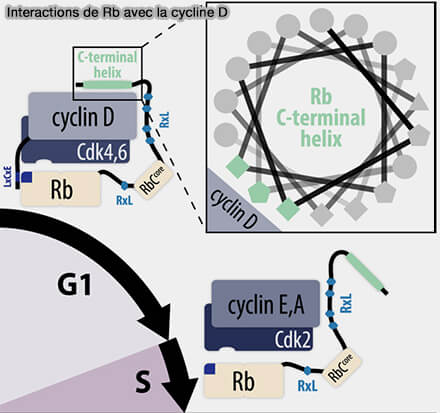
a. Les complexes cycline D/CDK4-6 phosphorylent la protéine Rb ou pRb (retinoblastoma protein), corepresseur transcriptionnel qui inhibait jusqu'à présent la progression du cycle cellulaire, ce qui libère le facteur de transcription E2F (Cyclin D-CDK4,6 Drives Cell-Cycle Progression via the Retinoblastoma Protein’s C-Terminal Helix 2019).
Le motif LxCxE de la cycline D est impliqué dans les interactions avec les protéines de la famille Rb, positionnant la cycline D comme plateforme de recrutement de substrats (
b. E2F active ensuite la transcription des gènes essentiels à la phase S codant :
- les enzymes de réplication de l’ADN, i.e. ADN polymérases et autres protéines de réplication (hélicases, primases, ligases), ainsi que les composants du complexe de pré‑réplicatif (ORC1, CDC6, CDT1, MCM2-7),
- la cycline E qui s'associe à CDK2 pour initier l’activation des origines de réplication et déclencher l’entrée en phase S,
- la cycline A qui s'associe à CDK2, pour maintenir les fourches de réplication et empêcher le re-licensing.
c. L’activité transcriptionnelle d’E2F est maximale en G1 tardive et au checkpoint G1/S, puis elle est progressivement éteinte au cours de la phase S par plusieurs mécanismes convergents, dont l’ubiquitination dépendante de SCFcycline F, la reconfiguration des complexes Rb/E2F, la répression chromatinienne et les boucles de rétrocontrôle négatif, garantissant l’arrêt strict du programme transcriptionnel G1/S.
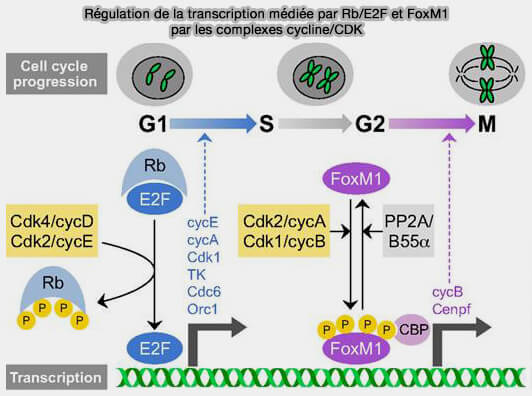
(Figure : vetopsy.fr d'après Lim et Kaldis)
c. Parallèlement, l'activité APC/CCdh1 s’éteint progressivement sous l’effet de l’activation croissante des complexes cycline D/CDK4-6, puis cycline E/CDK2, permettant à la cellule de franchir le point R et de préparer l’entrée en phase S.
Cette extinction libère définitivement le système cycline/CDK de son frein mitotique résiduel et permet à la cellule de franchir le point R.
4. Lorsque les signaux prolifératifs deviennent insuffisants ou qu’un stress cellulaire est détecté, la progression est interrompue par :
- l’activation des iCKI (CDK inhibitors), comme p21CIP1 et p27KIP1,
- par le maintien de Rb sous sa forme hypophosphorylée
- par les voies de contrôle de l’ADN, i.e. p53, ATR/Chk1 et ATM/Chk2).
Ces mécanismes empêchent l’activation des complexes cycline D/CDK4-6 ou cycline E/CDK2, bloquant la transition G1/S tant que les conditions ne sont pas restaurées.
| Étape | Acteurs principaux | Événements clés | Conséquence fonctionnelle |
|---|---|---|---|
| Sortie de mitose/ début de G1 |
|
|
|
| G1 précoce (état basal) |
|
|
Prévention de toute entrée prématurée en phase S |
| Signaux externes favorables |
|
Induction transcriptionnelle des cyclines D |
Autorisation de l'entrée progressive dans G1 |
| G1 intermédiaire (montée des cyclines D) |
Cycline D/CDK4-6 | Phosphorylation de Rb (hypo → hyperpartielle) |
Début de la levée de l'inhibition de Rb |
| Passage du point R |
|
|
Engagement irréversible vers la réplication |
| Induction cycline E |
E2F ➞ cycline E/CDK2 |
|
Préparation directe de l'entrée en S |
| Extinction progressive de Cdh1 |
|
Disparition du frein APC/CCdh1 |
Transition G1 → S pleinement engagée |
| G1 tardive ➞ phase S |
Cycline E/CDK2 | Activation des complexes de réplication |
|
Phase S : réplication génétique
La phase S (de l'anglais, synthesis, synthèse) correspond à la réplication complète du matériel génétique (2n, 4c).
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


