Constituants cellulaires
Cytosquelette : microtubules
MAP : protéines associées aux microtubules
MAP organisatrices
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Matrice extracellulaire
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Les MAP organisatrices structurent le réseau microtubulaire en coordonnant localement la stabilité, l’orientation et l’intégration des microtubules selon le contexte cellulaire, sans en contrôler directement la nucléation ou la dynamique intrinsèque.
MAP organisatrices
Les MAP associent des domaines structurés de liaison à la tubuline et des régions flexibles modulant leur affinité.
1. Cette organisation leur permet de maintenir la paroi microtubulaire dans un état stable malgré les fluctuations mécaniques.
- Les régions intrinsèquement désordonnées assurent une interaction multipoint amortissant les contraintes latérales.
- Les modules structurés reconnaissent des surfaces spécifiques de la tubuline α/β.
- L’architecture hybride guide la forme locale des protofilaments et soutient leur cohésion.
2. La combinaison flexibilité-structure garantit la stabilité du polymère en conditions dynamiques.
PRC1
PRC1 (Protein Regulator of Cytokinesis 1) façonne les faisceaux antiparallèles du fuseau central et crée un échafaudage mécanique robuste indispensable à l’organisation de la zone médiane.
1. PRC1 organise et stabilise les microtubules interpolaires.
- Elle reconnaît les microtubules antiparallèles et les maintient côte à côte, formant des faisceaux alignés qui stabilisent la zone médiane du fuseau (faisceautage).
- Cette organisation maintient une géométrie stable du fuseau central, condition nécessaire à son allongement et à sa cohésion.
2. PRC1 définit une plateforme structurale pour la phase anaphasique.
- Le faisceautage assuré par PRC1 permet l’extension contrôlée du fuseau en anaphase B.
- Il fournit un support mécanique au recrutement coordonné des moteurs et régulateurs associés à la zone médiane (midzone) du fuseau (
rôles de PCR1).
Remarque : PRC1 (Protein Regulator of Cytokinesis 1) n'a rien à voir avec PRC1 (Polycomb Repressive Complex 1), complexe épigénétique nucléaire dont la fonction principale est la répression transcriptionnelle via l’ubiquitination de l'histone H2A.
TPX2
TPX2 est une MAP organisatrice périchromosomique dont l’activité est spatialement contrôlée par le gradient Ran-GTP, jouant un rôle central dans l’organisation, la densité et la cohérence architecturale du fuseau mitotique (TPX2 2017).
TPX2 (Targeting Protein for Xklp2) doit son nom à sa capacité à cibler Xklp2, une kinésine mitotique identifiée chez Xenopus impliquée dans l’organisation du fuseau, dont l’équivalent fonctionnel chez les mammifères correspond à des kinésines de la famille de la kinésine-12, telles que KIF15.
Activation des MAP par RAN-GTP
Ran-GTP est une petite GTPase dont la fonction centrale en mitose est de créer une asymétrie spatiale autour des chromosomes.
Cette asymétrie ne repose pas sur une force mécanique, mais sur une différence locale d’état moléculaire.
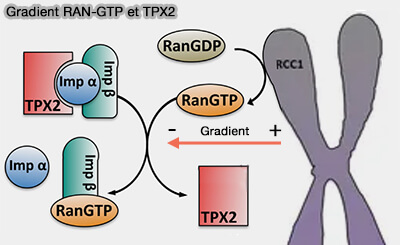
(Figure : vetopsy.fr d'après Garrido et Vernos)
1. RCC1 (Regulator of Chromosome Condensation 1) est une protéine chromatinienne constitutive, associée aux nucléosomes via les histones H2A/H2B, et agit comme facteur d’échange nucléotidique (GEF) de Ran (Non-centrosomal TPX2-Dependent Regulation of the Aurora A Kinase: Functional Implications for Healthy and Pathological Cell Division 2016).
- En mitose, la rupture de l’enveloppe nucléaire expose l’activité GEF chromatinienne de RCC1 au Ran cytosolique, générant une concentration élevée de Ran-GTP au voisinage immédiat des chromosomes,
- Celle-ci décroît progressivement avec la distance par reconversion en Ran-GDP, établissant ainsi un gradient radial périchromosomique stable, maintenu tant que la chromatine reste accessible, i.e. l’enveloppe nucléaire est absente.
2. Le gradient Ran-GTP ne déclenche pas directement la polymérisation des microtubules, mais contrôle l’état d’activation des protéines régulées par les importines (Interaction of spindle assembly factor TPX2 with importins-α/β inhibits protein phase separation 2021).
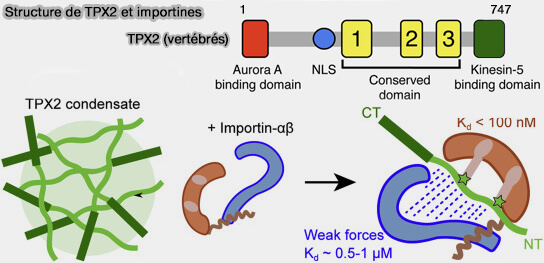
(Figure : vetopsy.fr d'après Safari et coll)
a. Dans le cytosol, de nombreuses MAP sont séquestrées par les complexes importine-α/β, ce qui les maintient inactives, notamment :
- TPX2, dont l’activité organisatrice est strictement dépendante de sa libération locale,
- HURP, impliquée dans la stabilisation périchromosomique des microtubules (HURP facilitates spindle assembly by stabilizing microtubules and working synergistically with TPX2 2024),
- NuMA, nécessaire à l’organisation des pôles du fuseau,
- certaines kinésines mitotiques et régulateurs associés au fuseau, comme KIF11/Eg5, KIF15, HSET/KIFC1 ou des cofacteurs de NuMA, dont l’activité et la localisation sont modulées indirectement par le gradient Ran-GTP.

(Figure : vetopsy.fr d'après Valdez et coll)
b. À proximité des chromosomes, Ran-GTP dissocie ces complexes, libérant localement ces MAP et restreignant leur activité à la région périchromosomique.

Ce mécanisme permet d’organiser le fuseau autour des chromosomes sans dépendre exclusivement du centrosome.
Rôles de TPX2
TPX2 agit comme une MAP organisatrice périchromosomique qui transforme l’activation locale dépendante de Ran-GTP en une architecture microtubulaire cohérente du fuseau (Microtubule nucleation for spindle assembly: one molecule at a time 2023).
Autour des chromosomes, les microtubules émergent de sources multiples et transitoires, avec des orientations initialement hétérogènes, ce qui peut conduire à un nuage instable et mal orienté, incompatible avec la bipolarité du fuseau mitotique.
1. TPX2 contribue à établir un environnement microtubulaire dense et structuré autour des chromosomes.
- TPX2 agit à ce stade par des interactions électrostatiques, réparties le long des microtubules, avec le lattice d'αβ-tubuline, qui augmentent la persistance locale des microtubules naissants sans figer leur dynamique.
- Cette stabilisation transitoire limite la perte prématurée des fibres nouvellement formées et permet l’émergence d’un réseau périchromosomique continu, condition préalable à son organisation ultérieure.
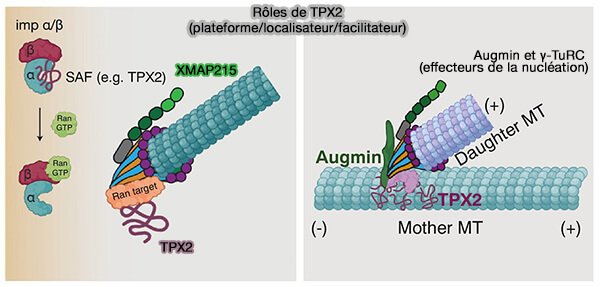
(Figure : vetopsy.fr d'après Kraus et coll)
2. TPX2 impose une cohérence géométrique et une orientation compatible avec la bipolarité du fuseau.
- Par ses interactions diffuses avec le lattice microtubulaire, TPX2 n’impose pas une contrainte mécanique directe mais favorise la persistance des microtubules dont l’orientation est compatible avec les axes du fuseau, tandis que les fibres mal orientées sont plus rapidement perdues.
- Ce mécanisme de sélection par persistance, plutôt que par faisceautage rigide, permet d’obtenir une orientation globale cohérente sans rigidifier prématurément l’architecture du fuseau.
3. TPX2 agit comme un nœud organisationnel coordonnant les activités locales sans s’y substituer.
TPX2 ne remplace ni les polymérases, ni les MAP stabilisatrices, ni les protéines de faisceautage, mais crée un contexte périchromosomique favorable dans lequel leurs activités deviennent efficaces et coordonnées.
a. En augmentant la persistance locale des microtubules en croissance, TPX2 facilite leur prise en charge par les facteurs d’élongation tels que XMAP215/ch-TOG et par les MAP stabilisatrices, ce qui accroît la densité fonctionnelle du réseau autour des chromosomes et favorise la stabilisation progressive des attachements kinétochoriens sans figer la dynamique (Complementary activities of TPX2 and chTOG constitute an efficient importin-regulated microtubule nucleation module 2016).
b. En préparant un contexte géométrique et mécanique compatible avec le faisceautage, TPX2 permet ensuite l’intervention efficace des MAP organisatrices tardives, notamment PRC1 dans la zone médiane du fuseau, assurant une répartition homogène des microtubules et la transmission cohérente des forces par les moteurs mitotiques, i.e. kinésines, dynéine.

Par cette coordination locale des facteurs d’élongation, de stabilisation, de faisceautage et de motorisation, TPX2 garantit l’établissement et le maintien d’une densité microtubulaire compatible avec un fuseau mitotique fonctionnel.
Remarque : TPX2 est également connue comme cofacteur d’Aurora A, mais cette fonction kinase-dépendante relève de la régulation du fuseau mitotique.
NuMA
NuMA (Nuclear Mitotic Apparatus protein) est une protéine organisatrice majeure du fuseau mitotique, spécialisée dans la focalisation des pôles et la transmission des forces mécaniques générées par les moteurs.
1. NuMA concentre les l’extrémité (-) des microtubules vers les pôles et recrute la dynéine-1 et la dynactine constituant un module fonctionnel d’organisation polaire (NuMA and Ninein: Dynein Cargo-Adaptors Without a Classical Cargo 2025).
a. Cette organisation conduit à une focalisation des pôles, i.e. regroupement des microtubules en deux pôles compacts, condition indispensable à la stabilité et à la robustesse mécanique du fuseau.
b. Elle assure plusieurs autres fonctions.
- La cohésion mécanique du fuseau est maintenue par le regroupement des microtubules polaires, ce qui stabilise l’architecture bipolaire.
- L’alignement vectoriel des forces est rendu possible par le recrutement coordonné de moteurs.
- La transmission des tensions générées par la dynéine permet d’absorber les contraintes imposées par l’attachementset la traction sur les chromosomes.
2. NuMA joue également un rôle central dans la génération des forces corticales qui positionnent le fuseau dans la cellule.
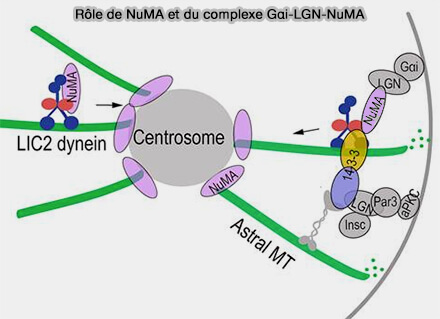
(Figure : vetopsy.fr d'après Mahale et coll)
a. La dynéine corticale n’est pas ancrée directement à la membrane plasmique et son recrutement repose sur un complexe tripartite d’ancrage cortical fonctionnellement conservé.
- Gαi est une sous-unité α d’une protéine G hétérotrimérique, ancrée à la membrane plasmique par myristoylation et palmitoylation, qui définit des domaines corticaux compétents pour la traction du fuseau.
- LGN (GPSM2) est un adaptateur cytosolique qui se lie à Gαi via ses domaines GoLoco et sert d’interface entre la membrane et les effecteurs mécaniques.
b. NuMA est recrutée au cortex par le complexe Gαi-LGN et se lie aux microtubules astraux et au complexe dynéine/dynactine.
Remarque : la figure ci-contre montre que l’interaction avec 14-3-3 implique le complexe dynéine–LIC2, et non une liaison directe de NuMA à 14-3-3.
3. Ce module permet plusieurs propriétés fonctionnelles.
- l’ancrage spatialement contrôlé de la dynéine au cortex,
- la conversion de l’activité motrice de la dynéine en forces de traction sur les microtubules astraux,
- le positionnement, l’orientation et la stabilisation du fuseau mitotique en métaphase et en anaphase B.
Complexe augmine
L'augmine amplifie le réseau en recrutant la γ-tubuline sur les microtubules préexistants.
1. Elle génère une ramification latérale indispensable à la densité du fuseau.
- La nucléation latérale augmente le nombre de fibres sans passer par les centrosomes.
- La ramification renforce la compacité et la rigidité du fuseau.
- Le maillage dense optimise la capture et la séparation des chromosomes.
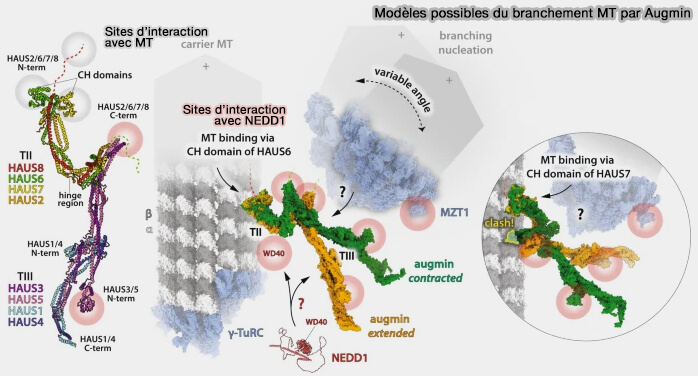
(Figure : vetopsy.fr d'après Manka)
2. L'augmine contribue à l’architecture interne du fuseau mitotique.

L'augmine est étudiée dans le chapitre spécifique sur les nucléations lors du cycle cellulaire.
SSNA1
SSNA1 (Sjögren Syndrome Nuclear Autoantigen 1), aussi appelée NA14/DIP13, est une MAP organisatrice atypique impliquée dans la modulation locale de l’architecture microtubulaire.
1. SSNA1 est principalement monomérique et se lie directement au lattice des microtubules.
- Elle interagit avec le lattice d'αβ-tubuline, et stabilise les microtubules dynamiques.
- Elle modifie leur comportement cinétique, en ralentissant à la fois la croissance et la dépolymérisation.
- Elle reste préférentiellement associée aux microtubules nouvellement formés, où elle module leur devenir structural (SSNA1 stabilizes dynamic microtubules and detects microtubule damage 2021).
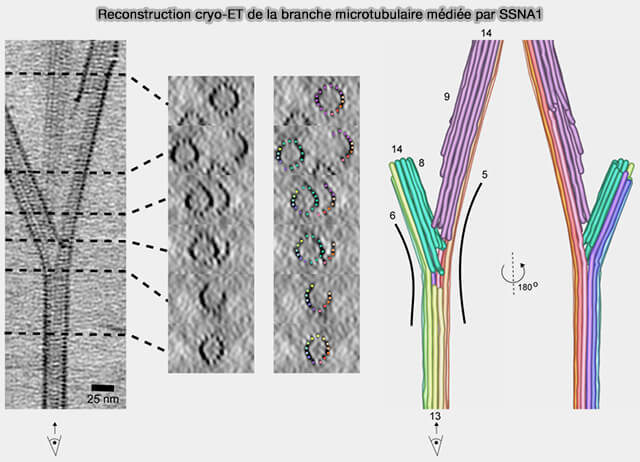
(Figure : vetopsy.fr d'après Basnet et coll)
2. SSNA1 influence la géométrie locale du réseau microtubulaire.
a. En guidant la courbure initiale des protofilaments, SSNA1 induit des déviations progressives de trajectoire du polymère existant, sans recruter le complexe γ-TuRC, ni initier de nucléation secondaire (Direct induction of microtubule branching by microtubule nucleation factor SSNA1 2018).
Ces configurations évoquant des " branchements " correspondent ainsi à des réorientations locales ou à des changements de direction continus d’un même microtubule, et non à la formation de microtubules fils indépendants comme dans le cas de l’augmine.
b. Cette activité est particulièrement marquée dans les neurones et dans les zones de remodelage cytosquelettique actif, où SSNA1 contribue à une diversification locale de l’architecture microtubulaire par modulation géométrique du lattice, plutôt qu’à une amplification quantitative du réseau.
MAP7 (ensconsin)
MAP7 (ensconsin) est une MAP organisatrice qui ne contrôle pas directement la nucléation ou la stabilité intrinsèque des microtubules, mais oriente fonctionnellement le réseau en couplant organisation microtubulaire et transport moteur.
1. MAP7 se fixe le long du lattice microtubulaire et sert principalement de plateforme de recrutement et d’activation des kinésines, en particulier de la kinésine-1 (MAP7 family proteins regulate kinesin-1 recruitment and activation 2019).
- Elle augmente l’affinité de la kinésine-1 pour les microtubules.
- Elle favorise l’engagement processif des moteurs sur des microtubules longs, stables et post-traductionnellement modifiés, i.e. détyrosinés, caractéristiques des réseaux matures.
- Elle contribue ainsi à la polarisation fonctionnelle du réseau sans modifier directement la dynamique croissance-catastrophe (
dynamique des microtubules).
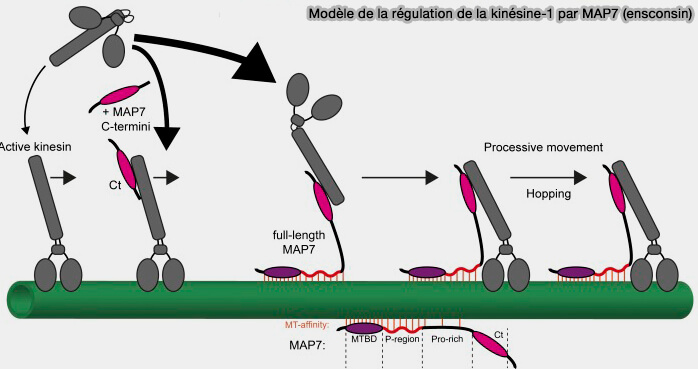
(Figure : vetopsy.fr d'après Hooikaas et coll)
2. Dans les cellules polarisées et les neurones, MAP7 participe à la sélection des microtubules utilisés pour le transport à longue distance, renforçant la spécialisation axonale et la distribution directionnelle des cargos.
MAP7 agit ainsi comme un coupleur fonctionnel entre architecture microtubulaire et transport moteur, orientant l’usage du réseau plutôt que sa dynamique intrinsèque.
Autres MAP
Les autres classes de MAP sont :
- les MAP stabilisatrices,
- les MAP déstabilisatrices,
- les MAP d'extrémité (+),
- les MAP d'extrémité (-).
Retour aux microtubules
Biologie cellulaire et moléculaireMembrane plasmiqueNoyauCytoplasmeMitochondriesSystème endomembranaireRéticulum endoplasmiqueAppareil de GolgiEndosomesLysosomesPeroxysomesProtéasomesCytosqueletteFilaments d'actineFilaments intermédiairesMicrotubulesTubulineDynamique des MicrotubulesNucléationFissionMAPCentrioleCentrosomeFuseau mitotiqueReproduction cellulaireBiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


