Cycle cellulaire
Reproduction cellulaire
Méiose : complexe synaptonémal
- Biologie cellulaire et moléculaire
- Constituants de la cellule
- Reproduction cellulaire
- Biochimie
- Transport membranaire
- Moteurs moléculaires

Le complexe synaptonémal est une structure protéique tripartite transitoire de la prophase I méiotique, indispensable à l’appariement, à la synapsis et au contrôle des recombinaisons entre chromosomes homologues.
Le complexe synaptonémal est une structure supramoléculaire transitoire, propre à la prophase I de la méiose, qui assure :
- l’alignement longitudinal des chromosomes homologues,
- la stabilisation de leur appariement,
- l’organisation fonctionnelle des chromosomes homologues en vue de la recombinaison.
Sa formation débute à la transition leptotène-zygotène, se généralise au pachytène et disparaît au diplotène, traduisant une dynamique strictement couplée à la progression méiotique.
Organisation structurale du complexe synaptonémal
Le complexe synaptonémal présente une organisation tripartite conservée, responsable de l’espacement régulier des chromosomes homologues et du maintien de la synapsis.

Vous pouvez lire : Meiotic Chromosome Structure, the Synaptonemal Complex, and Infertility (2023), article dans lequel les structures des différentes protéines sont développées.
1. Les deux éléments latéraux correspondent aux axes protéiques associés à chaque chromosome homologue et dérivent des axes axiaux formés au leptotène.
- Ils sont constitués principalement de SYCP2 et SYCP3, protéines fibrillaires capables d’auto-assemblage longitudinal.
- Ils assurent l’ancrage des boucles de chromatine et servent de plateforme structurale pour l’organisation méiotique.
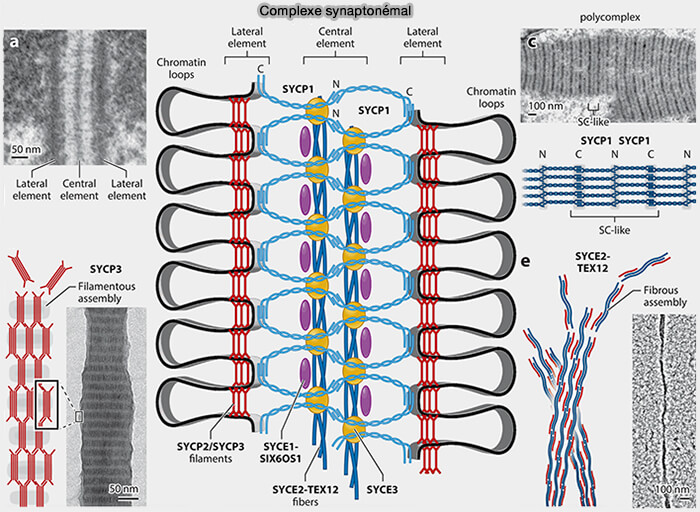
(Figure : vetopsy.fr d'après Adams et Davies)
2. Les filaments transverses relient les deux éléments latéraux et sont formés majoritairement par SYCP1.
La protéine adopte une organisation polarisée qui impose une distance inter-homologues constante et stabilise la synapsis.
- Le domaine C-terminal s’ancre dans les éléments latéraux.
- Le domaine N-terminal s’associe dans la région médiane.
3. L’élément central qui occupe la région médiane du complexe est constitué de SYCE1, SYCE2, SYCE3, TEX12 et SIX6OS1.
Ces protéines forment une plateforme structurale coopérative indispensable à la stabilité et à la fonctionnalité du complexe au pachytène, l’invalidation d’un seul composant majeur suffisant à désorganiser l’ensemble de la structure.
Dynamique d’assemblage durant la prophase I
L’assemblage du complexe synaptonémal est strictement couplé aux sous-stades de la prophase I et suit une progression ordonnée qui permet (Tracking down the molecular architecture of the synaptonemal complex by expansion microscopy 2020) :
- la construction structurale nécessaire à l’appariement,
- la stabilisation indispensable à l’organisation de la recombinaison,
- le démantèlement requis pour permettre la ségrégation ultérieure.
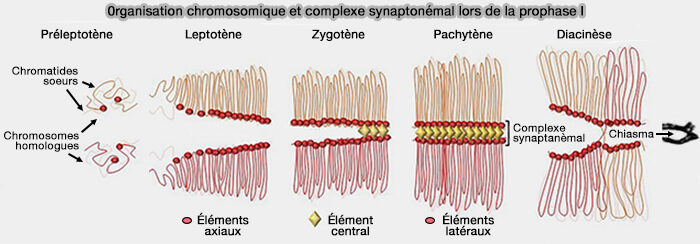
(Figure : vetopsy.fr d'après Grey et de Massy)
1. Au stade leptotène, les chromosomes s’individualisent et forment des axes axiaux.
Ces axes sont enrichis en SYCP2 et SYCP3 et constituent le précurseur structural des futurs éléments latéraux.
2. Au stade zygotène, l’appariement des chromosomes homologues débute.
- SYCP1 s’insère progressivement entre les deux axes.
- Les filaments transverses initient la synapsis sous forme de segments discontinus, qui s’étendent ensuite le long des chromosomes.
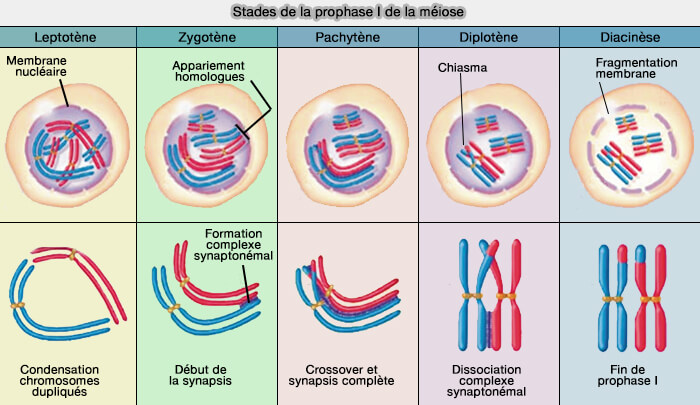
(Figure : vetopsy.fr)
3. Au stade pachytène, la synapsis est complète et le complexe synaptonémal est continu sur toute la longueur des homologues.
L’élément central est pleinement constitué, avec recrutement stable de SYCE1, SYCE2, SYCE3, TEX12 et SIX6OS1.

C’est au stade pachytène que la recombinaison méiotique est fonctionnellement organisée.
4. Au stade diplotène, le complexe synaptonémal se désassemble progressivement. SYCP1 et les protéines de l’élément central disparaissent.
Les homologues restent associés uniquement au niveau des points de crossing-over, visibles sous forme de chiasmas.
Rôle fonctionnel dans l’appariement des homologues
Le complexe synaptonémal assure la stabilisation de l’appariement entre chromosomes homologues sur toute leur longueur et repose sur la reconnaissance homologue initiée aux stades leptotène-zygotène.
1. La reconnaissance entre chromosomes homologues en prophase I repose sur trois mécanismes complémentaires.
- La mise en contact des chromosomes homologues dans le noyau repose sur la dynamique spatiale des chromosomes, liée au bouquet télomérique et aux mouvements dépendants du cytosquelette nucléaire, qui rend la reconnaissance homologue efficace.
- Les cassures double brin programmées génèrent des extrémités d’ADN simple brin servant de support moléculaire à la recherche d’homologie.
- Le choix préférentiel du chromosome homologue repose sur l’action des recombinases RAD51 et DMC1, qui utilisent les extrémités d’ADN simple brin pour tester la complémentarité de séquence avec l’ADN du partenaire homologue, en favorisant les échanges inter-homologues plutôt qu’inter-sœurs.
2. Ces processus agissent de concert pour rendre la reconnaissance efficace, avant l’installation complète du complexe synaptonémal, qui intervient ensuite comme facteur structural de stabilisation durable de l’appariement.
Rôle du complexe synaptonémal dans l’organisation des crossing-over
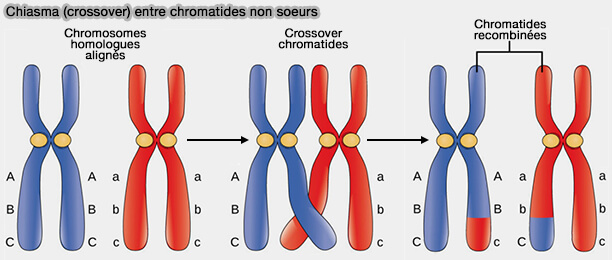
(Figure : vetopsy.fr d'après courses.lumenlearning.com)
Au-delà de sa fonction d’alignement, le complexe synaptonémal participe activement à la sélection, à la stabilisation et à l’organisation spatiale des événements de recombinaison conduisant aux crossing-over le long des chromosomes homologues (Recombination, Pairing, and Synapsis of Homologs during Meiosis 2015).
a. Lorsque la synapsis est complète au pachytène, le complexe synaptonémal constitue une plateforme structurale continue qui permet :
- l’intégration spatiale des sites de recombinaison,
- la sélection d’un nombre limité d’événements destinés à devenir des crossing-over,
- leur répartition régulière le long des chromosomes (interférence).
b. Cette fonction repose sur l’accumulation sélective de protéines de la machinerie de recombinaison le long du complexe synaptonémal (

L’altération du complexe synaptonémal perturbe ces processus et entraîne une diminution des crossing-over, une mauvaise répartition des chiasmas et une augmentation du risque d’erreurs de ségrégation en méiose I.
2. Chez les mammifères, des facteurs tels que RNF212 et HEI10, se concentrent sur un nombre limité de sites de recombinaison situés sur le complexe synaptonémal, ce qui a une conséquence fonctionnelle directe proche d’un phénomène de sélection par compétition de ressources (
La sélection d’un crossing-over à un endroit donné limite mécaniquement la formation d’événements trop proches et contribue à leur répartition régulière le long des chromosomes.
Ainsi, le complexe synaptonémal ne se limite pas à stabiliser l’appariement, mais contribue directement à l’organisation spatiale des crossing-over et à la sécurisation de la ségrégation des chromosomes homologues.
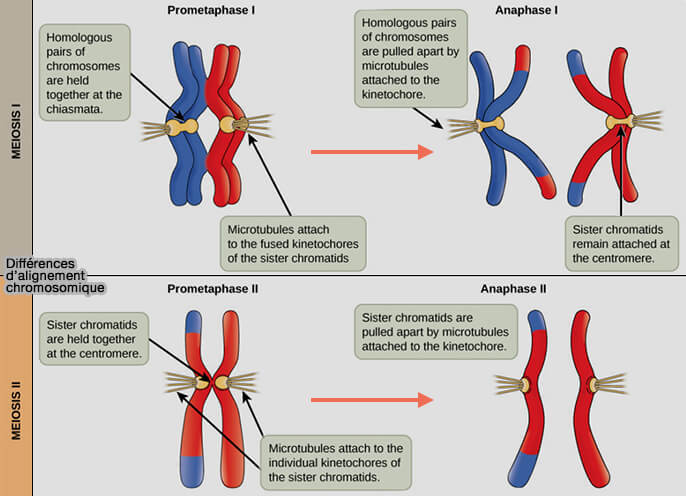
(Figure : vetopsy.fr d'après courses.lumenlearning.com)
Dissolution du complexe et conséquences pour la ségrégation
La disparition du complexe synaptonémal, qui débute au diplotène, constitue une étape structurante de la fin de la prophase I.
1. SYCP1 et les protéines de l’élément central se dissocient progressivement, tandis que les éléments latéraux persistent transitoirement sous forme d’axes résiduels.
- La perte du complexe libère les chromosomes homologues et leur association ne persiste plus qu’au niveau des chiasmas, qui matérialisent les crossing-over stabilisés.
- Ces chiasmas assurent la cohésion fonctionnelle de la paire de chromosomes homologues jusqu’à la métaphase I et permettent leur orientation correcte sur le fuseau méiotique et conditionnent leur disjonction réductionnelle.
2. Une dissolution anormale du complexe perturbe ce processus.
- Une disparition prématurée réduit la stabilité des chiasmas.
- Une persistance excessive interfère avec leur résolution correcte.
3. La dynamique de désassemblage du complexe synaptonémal participe ainsi directement au contrôle temporel et mécanique de la ségrégation des chromosomes homologues.
Retour vers la méiose
Biologie cellulaire et moléculaireConstituants de la celluleReproduction cellulaireMatériel génétiqueFuseauCycle cellulaireInterphasePhase G1Phase SPhase G2MitoseProphasePrométaphaseMétaphaseAnaphaseTélophaseCytokinèseAbcissionMéioseRégulation du cycle cellulaireCyclinesCDKComplexes Cyclines/CDKPoints de contrôles (checkponts)Enzymes mitotiquesMoteurs mitotiquesComplexes SMC (condensines et cohésines)BiochimieTransport membranaire Moteurs moléculairesVoies de signalisation


