Voies métaboliques
Pyruvate
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

L'acide pyruvique ($\ce{CH3COCOOH}$) est le plus simple des α-cétoacides, i.e. molécule comportant à la fois un groupe carboxylique ($\ce{R-COOH}$) et un groupe cétone ($\ce{R-C(=O)-R'}$).
Le pyruvate, sa base conjuguée ($\ce{CH3COCOO-}$), est un intermédiaire essentiel dans plusieurs voies métaboliques.
Enzymes intervenant dans le métabolisme du pyruvate
| Enzymes | Réaction | Symptômes lors de déficience |
|---|---|---|
| Pyruvate kinase (PK) | $\ce{Phosphoénolpyruvate + ADP}$ $\leftrightharpoons$ $\ce{pyruvate + ATP}$ |
|
| Lactate déshydrogénase (LDH) | $\ce{Pyruvate + NADH + H+}$ $\leftrightharpoons$ $\ce{L-lactate + NAD+}$ |
|
| Alanine transaminase (ALT) | $\ce{L-alanine + α-cétoglutarate}$ $\leftrightharpoons$ $\ce{pyruvate + L-glutamate}$ |
? |
| Enzyme malique à NADP | $\ce{(S)-malate + NADP+}$ |
? |
| Pyruvate carboxylase (PC) | $\ce{Pyruvate + HCO3- + ATP}$ $\longrightarrow$ $\ce{Oxaloacétate + ADP + Pi}$ |
|
| Pyruvate déshydrogénase (PDH) | $\ce{Pyruvate + CoA-SH + NAD+}$ $\longrightarrow$ $\ce{NADH + H+ + CO2 + Acétyl-CoA}$ |
|
| Pyruvate déshydrogénase kinase (PDK) | $\ce{PDH + ATP}$ -$\longrightarrow$ $\ce{P-PDH + ADP}$ |
? |
| Pyruvate déshydrogénase phosphatase (PDP) | $\ce{P-PDH-> PDH + Pi}$ | Très rare |
| Mitochondrial pyruvate carrier (MPC) | $\ce{Pyruvate_{InterMemb}}$ $\leftrightharpoons$ $\ce{pyruvate_{Matrice}}$ |
|
Biosynthèse du pyruvate
(Figure : vetopsy.fr)
Le pyruvate cytosolique peut provenir de différentes sources (Regulation of pyruvate metabolism and human disease 2014).
Sources principales
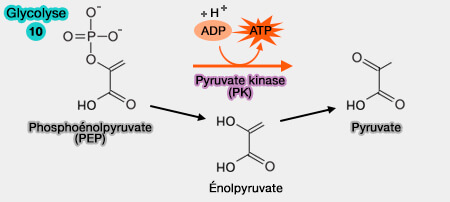
1. La source principale est sans conteste la glycolyse (
$\ce{Phosphoénolpyruvate + ADP}$ $\leftrightharpoons$ $\ce{énolpyruvate}$ $\leftrightharpoons$ $\ce{pyruvate + ATP}$
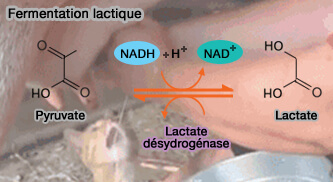
2. Le pyruvate est produit par l'oxydation du lactate par la lactate déshydrogénase ou LDH (
$\ce{Pyruvate + NADH + H+}$ $\leftrightharpoons$ $\ce{L-lactate + NAD+}$
(Figure : vetopsy.fr)
Autres sources
Acides aminés tricarbonés
Vue d'ensemble
L'alanine, la sérine, la thréonine, la glycine, la cystéine et le tryptophane peuvent également être convertis en pyruvate.
L'alanine est l'un des plus importants et un des principaux précurseurs de la gluconéogenèse.
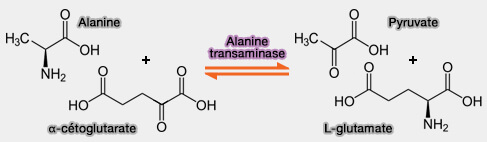
L'alanine transaminase (ALT ou pyruvate transaminase glutamique ou GPT), EC 2.6.1.2, catalyse la réaction suivante :
$\ce{L-alanine + α-cétoglutarate}$ $\leftrightharpoons$ $\ce{pyruvate + L-glutamate}$

L'alanine, l'α-cétoglutarate, le glutamate et le pyruvate sont des intermédiaires essentiels entre le métabolisme des glucides et des acides aminés.
(Figure : vetopsy.fr)
On retrouve deux isoformes d'ALT dont les expressions varient avec les espèces :
- ALT1 est située dans le cytosol des cellules du tissu adipeux brun et blanc, de l'intestin et du foie : cette isoforme est prédominante chez l'homme (Isoform-specific alanine aminotransferase measurement can distinguish hepatic from extrahepatic injury in humans 2012).
- ALT2 se trouve dans la matrice mitochondriale des cellules musculaires et cérébrales.
Cycle de l'alanine (cycle de Cahill ou glucose-alanine)
Le pyruvate et l'alanine sont les substrats centraux du cycle de l'alanine, appelé aussi cycle de Cahill ou cycle glucose-alanine, qui relie le métabolisme musculaire et hépatique.
- Dans le muscle, le pyruvate est transaminé en alanine et exporté dans le sang.
- Le foie récupère l'alanine et la désamine en pyruvate, ce qui favorise la gluconéogenèse, le cycle de Krebs et les multiples voies qui en dépendent.
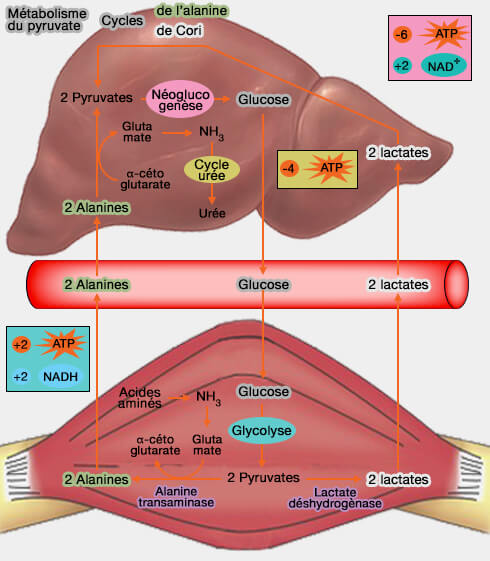
(Figure : vetopsy.fr)
Le cycle de l'alanine, semblable au cycle de Cori, se produit souvent parallèlement : il est moins efficace que lui (
| Caractéristique | Cycle de Cori | Cycle de Cahill (glucose-alanine) |
|---|---|---|
| Transporté vers le foie | Lactate | Alanine |
| Source de pyruvate | Glycolyse (pyruvate ➞ lactate) |
Glycolyse + transamination (pyruvate + glutamate ➞ alanine) |
| Rôle principal |
|
Transporter l'ammoniac vers le foie pour détoxification |
| Déchet azoté produit | Aucun | Urée |
| Conditions d'activation |
|
|
| Consommation hépatique | 6 ATP pour 1 glucose (gluconéogenèse) |
6 ATP pour 1 glucose + coût du cycle de l'urée |
1. Le glutamate est désaminé par la glutamate déshydrogénase (GLDH, GDH) créant de l'α-cétoglutarate (ou acide 2-oxoglutarique) et de l'ammoniac ($\ce{NH3}$).
$\ce{L-glutamate + H2O + NAD+}$ $\leftrightharpoons$ $\ce{α-cétoglutarate + NH3 + NADH + H+}$ par EC 1.4.1.2.
$\ce{L-glutamate + H2O + NAD(P)+}$ $\leftrightharpoons$ $\ce{α-cétoglutarate + NH3 + NAD(P)H + H+}$ par EC 1.4.1.3.
$\ce{L-glutamate + H2O + NADP+}$ $\leftrightharpoons$ $\ce{α-cétoglutarate + NH3 + NADPH + H+}$ par EC 1.4.1.4.
2. Cette réaction produit de l'ammoniac ($\ce{NH3}$) qui doit être éliminée par le cycle de l'urée qui consomme 3 ATP (Nitrogen Excretion and the Urea Cycle) : le rendement énergétique s'en ressent !
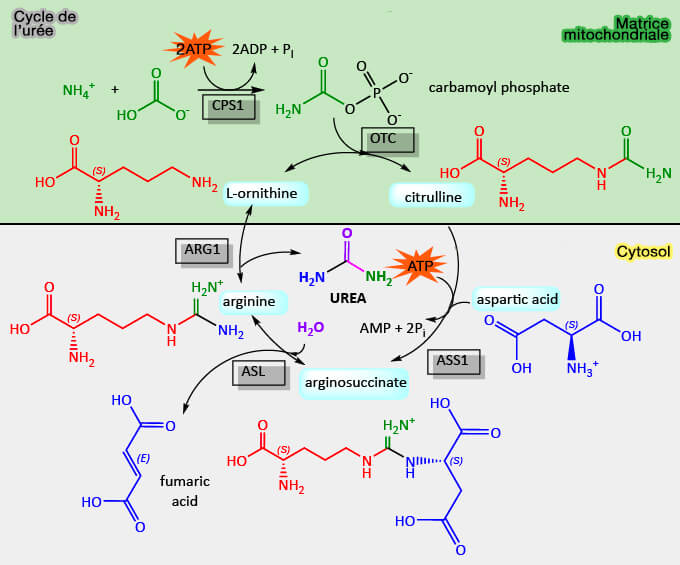
(Figure : vetopsy.fr d'après Jakubowski et Flatt)
3. Par contre, le cycle de Cahill ne consomme pas de NADH.
Le cycle de l'alanine nécessite la présence d'alanine transaminase, qui ne se trouve que dans les muscles, le foie et les intestins.
Ce cycle est donc utilisé à la place du cycle de Cori :
- lorsque l'ammoniac ($\ce{NH3}$) doit être détoxiqué par le foie,
- lors de dégradation musculaire, i.e. catabolisme des acides aminés musculaires.
Malate
Le pyruvate peut être reformé à partir du malate par l'enzyme malique à NADP cytosolique (NADP-malic enzyme - NADP-ME - ou malate dehydrogenase (oxaloacetate-decarboxylating) (NADP+) ou pyruvic-malic carboxylase), EC 1.1.1.40 :
$\ce{(S)-malate + NADP+}$ $\leftrightharpoons$ $\ce{pyruvate + CO2 + NADPH}$
Cette enzyme est essentielle pour la circulation des métabolites mitochondriaux du cycle de Krebs comme le citrate, le malate et l'oxaloacétate entre le cytosol et les mitochondries.
Devenir du pyruvate
Le devenir du pyruvate diffère selon l'accepteur d'électrons externe disponible et dépend du métabolisme cellulaire.
En aérobiose
En aérobiose, i.e. avec de $\ce{O2}$, i.e. en présence d'une chaîne respiratoire de transport d'électrons, le pyruvate peut subir :
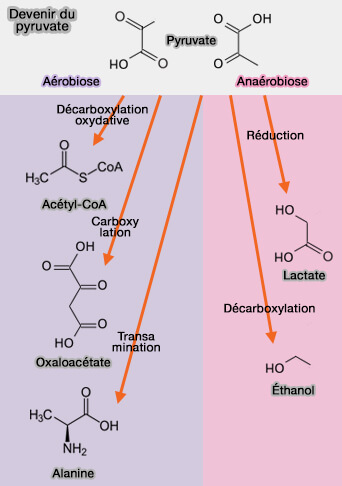
(Figure : vetopsy.fr)
1. une décarboxylation oxydative irréversible pour former de l'acétyl-CoA grâce au complexe pyruvate déshydrogénase (
$\ce{Pyruvate + CoA-SH + NAD+}$
->
$\ce{NADH + H+ + CO2 + Acétyl-CoA}$
2. une carboxylation pour former de l'oxaloacétate qui entre aussi dans le cycle de Krebs (
$\ce{Pyruvate +HCO3- + ATP}$
$\leftrightharpoons$
$\ce{oxaloacétate + ADP + Pi}$

Ces deux réactions sont primordiales car le pyruvate mitochondrial ne sert pas uniquement à la production d'ATP, mais fournit également le carbone à plusieurs voies biosynthétiques majeures qui transitent par le cycle de Krebs.
Ces deux enzymes se trouvent dans la matrice mitochondriale, i.e. le pyruvate doit traverser les deux membranes mitochondriales, externe et interne par des canaux, respectivement par les VDAC (Voltage Dependent Anion Channel) et le MPC (Mitochondrial Pyruvate Carrier).
3. une transamination pour former de l'alanine (
$\ce{pyruvate + L-glutamate}$ $\leftrightharpoons$ $\ce{L-alanine + α-cétoglutarate}$
En anaérobiose
En anaérobiose, i.e. sans $\ce{O2}$, le pyruvate est réduit au cours de fermentations conduisant essentiellement :
- au lactate (
fermentation lactique), voie d'une importance primordiale à l'origine de nombreuses pathologies,
- à l'éthanol (
fermentation alcoolique).


