Glucides
Nucléotides-oses
Interconversion des oses
- Biochimie
- Chimie organique
- Bioénergétique
- Composition de la matière vivante
- Transport membranaire
- Moteurs moléculaires
- Voies de signalisation

Les nucléotides-oses (nucleotide sugars en anglais) sont des nucléotides liés à des oses qui, entre autres, interviennent dans l'interconversion des oses.
Les nucléotides-oses interviennent :
- dans l'interconversion entre oses,
- comme donneur d'unités glycidiques lors de :
- la biosynthèse des osides,
- la glucurono-conjugaison traitée avec les acides uroniques,
- la glycosylation des protéines, traitée dans des chapitres spécifiques.
Remarque : l'autre donneur d'unités glucidiques est le dolichol phosphate.
Interconversion des oses
Les nucléotides-oses interviennent dans des réactions d'interconversion des oses, i.e. on donnera chaque fois des exemples.
Épimérisation
1. La transformation réversible de l'UDP-galactose en UDP-glucose en est un bon exemple.
Le galactose, épimère en 4 du glucose, est le deuxième ose le plus répandu après le glucose.
a. L'épimérisation du galactose sur C4, catalysée par l'UDP-galactose-4 épimérase, UDP-glucose-4 épimérase ou GALE (EC 5.1.3.2) en présence de NAD, s'effectue en quatre étapes.
-
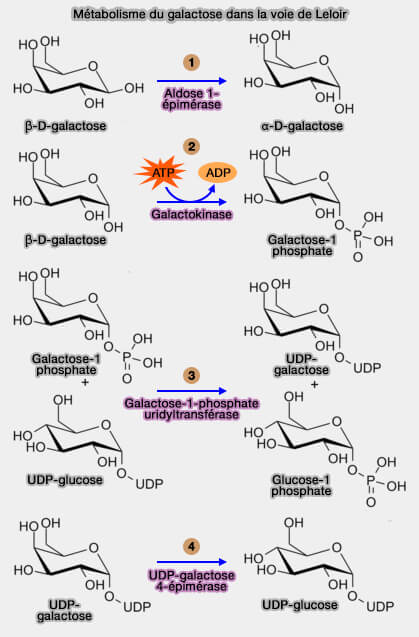
Métabolisme du galactose dans la voie de Leloir
(Figure : vetopsy.fr) - 2. La galactokinase (EC 2.7.1.6) phosphoryle ensuite l'α-D-galactose au niveau du groupe hydroxyle 1 pour produire du galactose-1-phosphate.
- 3. La galactose-1-phosphate uridylyltransférase (EC 2.7.7.12) catalyse le transfert réversible d'un fragment UMP de l'UDP-glucose au galactose-1-phosphate, générant de l'UDP-galactose et du glucose-1-phosphate.
- 4. L'UDP-glucose est régénéré à partir de l'UDP-galactose par GALE, i.e. l'UDP-glucose revient à l'étape 3. En tant que tel, GALE régénère un substrat nécessaire au cycle continu de la voie de Leloir.
b. Le glucose-1-phosphate généré à l'étape 3 peut être isomérisé en glucose-6-phosphate par la phosphoglucomatase (EC 5.4.2.2).
- Le glucose-6-phosphate entre facilement dans la glycolyse, conduisant à la production d'ATP et de pyruvate.
- Le glucose-6-phosphate peut être converti en inositol-3-phosphate par l'inositol-3-phosphate synthase (EC 5.5.1.4), générant un précurseur nécessaire à la biosynthèse de l'inositol ou myo-inositol $\ce{C6H12O6}$.
Le myo-inositol joue un rôle important comme messager secondaire dans les cellules eucaryotes, notamment sous forme d'inositol phosphate, dont l'inositol trisphosphate, InsP3 ou IP3, de phosphatidylinositol (PtdIns) et de phosphatidylinositol phosphates ou phosphoinositides (PIP).
2. Une réaction similaire convertit l'acide UDP-glucuronique en acide UDP-galacturonique (
Oxydation et décarboxylation de l'UDP-glucose
1. L'UDP-glucose est transformé en UDP-acide glucuronique (UDP-GlcA) au cours d'une réaction catalysée par l'UDP-glucose 6-déshydrogénase (EC 1.1.1.22) en présence de NAD (
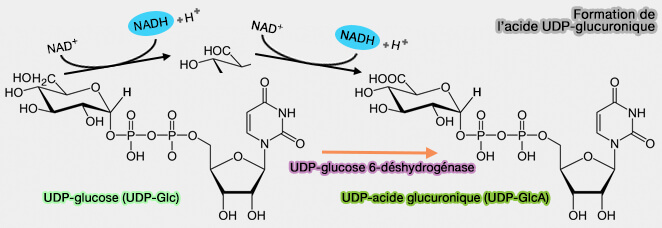
(Figure : vetopsy.fr)
2 . Une réaction similaire transforme le GDP-mannose en GDP-mannuronique.
Remarque : les autres acides uroniques naturels, i.e. acides galacturonique et iduronique, proviennent de l'épimérisation de l'acide UDP-glucuronique respectivement sur le carbone 4 et 5.
3. La décarboxylation de l'UDP-glucose, au cours d'une réaction catalysée par l'UDP-xylose synthase ou UDP-GlcUA décarboxylase (EC 1.1.1.305), conduit à l'UDP-xylose (Structure and Mechanism of Human UDP-xylose Synthase 2012).
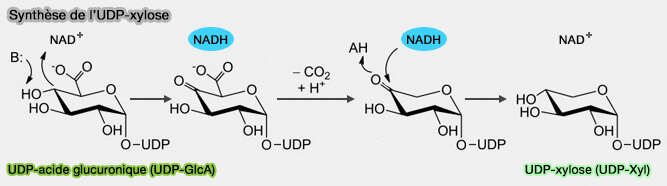
(Figure : vetopsy.fr d'après Eixelsberger et coll)
Réductions
Les réactions de réduction synthétisent les 6-désoxyoses.
- le L-fucose à partir du GDP-mannose,
- le L-rhamnose à partir de l'UDP-glucose.


