Domaines protéiques
Domaines von Willebrand (VW)

Le facteur de von Willebrand (VWF ou vWF) est constitué de plusieurs domaines dont l'un des plus significatifs est le domaine de type A (VWA), prototype d'une superfamille protéique.
Le VWF est essentiel à l'hémostase primaire (Facteur Willebrand et maladie de Willebrand : prérequis au diagnostic 2014).
Domaine von Willebrand A (VWA)
Vue d'ensemble
Le domaine von Willebrand A (VWA) est un domaine impliqué dans les interactions protéine-protéine qui est contenu dans plus de 500 protéines (Distribution and Evolution of von Willebrand/Integrin A Domains: Widely Dispersed Domains with Roles in Cell Adhesion and Elsewhere 2002).
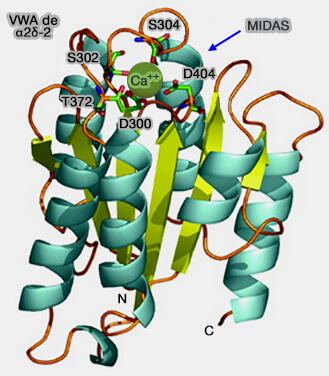
(Figure : vetopsy.fr d'après Canti)
1. Bien que la majorité de ces protéines soit extracellulaire, les plus anciennes, présentes chez tous les eucaryotes, sont toutes intracellulaires
Elles sont impliquées dans des fonctions telles que la transcription, la réparation de l'ADN, le transport ribosomique et membranaire et le protéasome (hélicases, chélatases, copines…).
2. Les autres, extracellulaires, sont impliquées dans l'adhésion cellulaire et les interactions avec les protéines de la matrice extracellulaire, et en particulier :
- les intégrines β (domaines I),
- huit des 28 types de collagène, i.e. VI, VII, XII, XIV, XX, XXI, XXII, and XXVIII (Collagens 2010 et Collagen VI at a glance 2015)
- d'autres protéines de la matrice extracellulaire comme les matrilines, la cochline/vitrine…
- des régulateurs de protéases tels que les facteurs de complément (B, C2, CR3 et CR4) ou les inhibiteurs de la trypsine,
- les sous-unités α2δ des canaux calcium voltage-dépendants Cav1 (type L) et Cav2 (types P/Q, N et R)…
3. Un certain nombre de maladies humaines proviennent de mutations dans les domaines VWA.
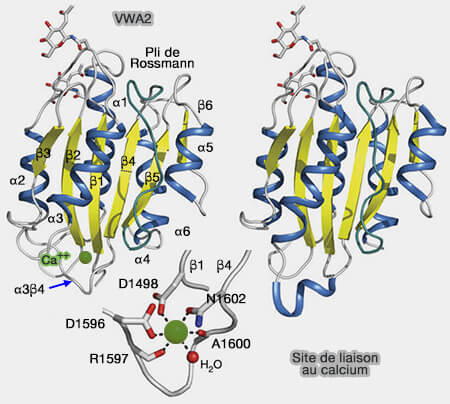
(Figure : vetopsy.fr d'après Jakobi)
Structure de VWA
1. Les domaines Von Willebrand du facteur A (VWA), domaines globulaires, comprennent environ 200 résidus d'acides aminés (Complement and the Multifaceted Functions of VWA and Integrin I Domains 2006).
- Ils adoptent un pli de Rossmann avec une feuille β centrale entourée d'hélices α amphipathiques.
- Les extrémités N- et C-terminales sont proches l'une de l'autre et la structure est souvent stabilisée par deux cystéines terminales qui forment un pont disulfure.
La structure du VWA du collagène VI montre des extensions C-terminales qui placent les extrémités N et C aux extrémités opposées (A Structure of a Collagen VI VWA Domain Displays N and C Termini at Opposite Sides of the Protein 2014).
2. Les domaines VWA contiennent le plus souvent un motif MIDAS (Metal Ion-Dependent Adhesion Site) qui est impliqué dans la liaison du ligand (Crystal Structure of the A Domain from the a Subunit of Integrin CR3 (CD11b/CD18) 1995 et Stable Coordination of the Inhibitory Ca2+ Ion at the Metal Ion-Dependent Adhesion Site in Integrin CD11b/CD18 by an Antibody-Derived Ligand Aspartate: Implications for Integrin Regulation and Structure-Based Drug Design 2011).
- La liaison du cation bivalent à ce motif module les changements conformationnels du domaine VWA à l'origine des fonctions variées suivant la protéine impliquée.
- Il implique la coordination du cation divalent par un anneau de cinq résidus polaires ou chargés (D-x-S-x-S) qui doit être complet ou " parfait ".
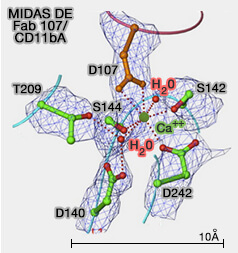
(Figure : vetopsy.fr d'après Mahalingam)
a. Dans les domaines de l'intégrine I, le motif MIDAS peut exister dans différents états d'activation avec des affinités variables aux ligands.
De plus, une modification conformationnelle du domaine I se produit lors de la liaison du ligand, dans laquelle l'hélice α7 C-terminale se déplace axialement vers l'extrémité C-terminale (Distinct roles of beta1 metal ion-dependent adhesion site (MIDAS), adjacent to MIDAS (ADMIDAS), and ligand-associated metal-binding site (LIMBS)s-binding sites in ligand recognition by integrin alpha2beta1 2008).
b. Certains domaines VWA, par exemple le facteur von Willebrand A3, se lient à leurs ligands par d'autres sites de liaison que le motif MIDAS (Identification of the Collagen-binding Site of the von Willebrand Factor A3-domain 2001).
Autres domaines von Willebrand
Dans le facteur de von Willebrand, on trouve aussi la suite de domaines suivante (Sequence and structure relationships within von Willebrand factor 2012 et von Willebrand factor: the old, the new and the unknown 2012) :
- selon l'ancienne version : D1-D2- D’-D3-A1-A2-A3-D4-B1-B2-B3-C1- C2-CK
- selon la nouvelle : D1-D2- D’-D3-A1-A2-A3-D4-C1-C2-C3-C4-C5-C6-CK.
1. Les domaines D1, D2, D’ et D3 sont impliqués dans le processus de multimérisation de la protéine.
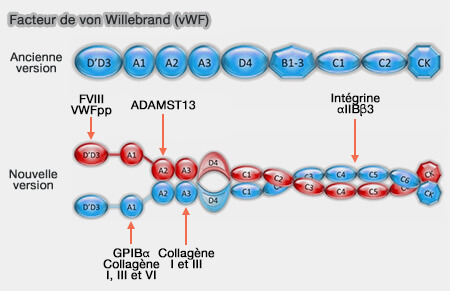
(Figure : vetopsy.fr d'après Fressinaud)
a. Le propeptide est formé par les domaines D1 et D2 et est indispensable à la multimérisation et au stockage du VWF.
b. Les domaines D’ et D3 contiennent 51 cystéines pour des ponts disulfure (intra-chaînes pour D’ et interchaînes pour D3 pour la multimérisation.
Les domaines D’ et D3 comportent aussi des sites de liaison du VWF au facteur VIII (FVIII).
2. Les domaines A1 et A3 possèdent des sites de liaison au collagène : collagène de type I, III et VI pour A1 et collagène de types I et III pour t A3.
Le domaine A1 est très important pour sa fonction, puisqu’il contient les sites de liaison pour la glycoprotéine Ibα plaquettaire (GPIbα).
3. Le domaine C1 permet l’interaction du vWF avec un récepteur plaquettaire, la GPIIb/IIIa (intégrine αIIbβ3).
vWF possède 232 résidus cystéines, douze chaînes N-glycosylées et dix O-glycosylées.
Retour aux domaines protéiques
Biologie cellulaire et moléculaireConstituants de la celluleMatrice extracellulaireReproduction cellulaireBiochimieChimie organiqueBioénergétiqueProtidesAcides aminésProtéinesDomaines protéiquesModifications post-traductionnelles des protéinesDégradations des protéinesUbiquitinationGlucidesLipidesEnzymesCoenzymesVitaminesHormonesTransport membranaireMoteurs moléculairesVoies de signalisation


